
| A、K+、OH-、NO3-、Cl- |
| B、H+、Na+、CO32-、Cl- |
| C、H+、K+、NO3-、Cl- |
| D、Cu2+、H+、Cl-、SO42- |


科目:高中化学 来源: 题型:
| 选项 | 电解质 | 纯净物 | 碱性氧化物 | 酸性氧化物 |
| A | 酒精溶液 | 冰水混合物 | CaO | SO2 |
| B | BaSO4 | 液氯 | Fe2O3 | CO2 |
| C | Fe(OH)3 | CuSO4?5H2O | Al2O3 | SO2 |
| D | NH3 | 水银 | CuO | NO2 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
 甲烷水蒸气重整制合成气是利用甲烷资源的途径之一,该过程的主要反应是
甲烷水蒸气重整制合成气是利用甲烷资源的途径之一,该过程的主要反应是| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2CO3比NaHCO3的溶度大 |
| B、受热时NaHCO3比Na2CO3稳定 |
| C、澄清的石灰水能与Na2CO3反应而不与NaHCO3反应 |
| D、向相同浓度的NaHCO3与Na2CO3溶液中分别滴入2滴酚酞溶液,前者红色更深 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该反应不属于氧化还原反应 |
| B、该反应中氧化剂是N2O4 |
| C、该反应中只有氮元素被氧化 |
| D、N2O4在反应过程中发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,46 g 红棕色二氧化氮气体中含有N、O原子个数和为3NA |
| B、标准状况下,1 NA CH3Cl所占的体积约为22.4 L |
| C、N2(g)+3H2(g)?2NH3(g)△H=-a kJ/mol,现向一密闭容器中通入2 NA个氨气分子反应完全后,吸收a kJ热量 |
| D、足量铜与1 L 18mol?L-1浓硫酸反应可以得到SO2的分子总数小于9 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
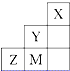
| A、电负性:Y>Z>M |
| B、离子半径:M->Z2->Y- |
| C、ZM2分子中各原子的最外层均满足8电子稳定结构 |
D、Z元素基态原子最外层电子排布图为 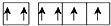 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 Ⅰ.常温下ClO2是黄绿色,有刺激性气味的气体,液态呈红棕色,熔点为-59℃,沸点为11.0℃;
Ⅰ.常温下ClO2是黄绿色,有刺激性气味的气体,液态呈红棕色,熔点为-59℃,沸点为11.0℃;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com