
【题目】下列溶液中有关物质的量浓度关系不正确的是( )
A.25℃时,0.1molL-1Na2CO3溶液中水电离出来的c(OH-)大于0.1molL-1NaOH溶液中水电离出来的c(OH-)
B.已知25℃时Ksp(AgCl)=1.8×10-10,则在0.3molL-1 NaCl溶液中,Ag+的物质的量浓度最大可达到6.0×10-10 molL-1
C.室温下,0.1molL-1NaHA溶液的pH=4,则有c(HA-)>c(H+)>c(H2A)>c(A2-)
D.pH相等的NaOH、CH3COONa和NaHCO3三种溶液,则有c(NaOH)<c(NaHCO3)<c(CH3COONa)
【答案】C
【解析】
A. 酸或碱抑制水的电离,含有若离子的盐促进水的电离;
B. 根据溶度积常数计算c(Ag+);
C. 室温下,0.1mol/LNaHA溶液的pH=4,说明HA-的电离程度大于水解程度;
D. pH相等的三种物质,NaOH的碱性最强,浓度最小,CH3COONa和NaHCO3中酸根离子水解程度越大,其浓度越小。
A. 酸或碱抑制水的电离,含有若离子的盐促进水的电离,所以25℃时,0.1mol/L Na2CO3溶液中水电离出来的c(OH-)大于0.1mol/L NaOH溶液中水电离出来的c(OH-),A项正确,不符合题意;
B. c(Ag+)=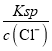 =
=![]() =6.0×10-10mol/L,B项正确,不符合题意;
=6.0×10-10mol/L,B项正确,不符合题意;
C. 室温下,0.1mol/LNaHA溶液的pH=4,说明HA-的电离程度大于水解程度,水电离生成H+,因此溶液中离子浓度大小顺序是c(HA-)>c(H+)> c(A2-) > c(H2A),C项错误,符合题意;
D. pH相等的三种物质,NaOH的碱性最强,浓度最小,水解程度CH3COO-<HCO3-,酸根离子水解程度越大,其浓度越小,所以这三种物质浓度大小顺序为c(NaOH)<c(NaHCO3)<c(CH3COONa),D项正确,不符合题意;
答案选C。


 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,在一容器内进行某一反应,M、N的物质的量随反应时间变化的曲线如下图所示,则下列叙述中,正确的是( )
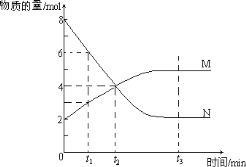
A. 反应的化学方程式一定为2M![]() N
N
B. ![]() 时,逆反应速率一定大于正反应速率
时,逆反应速率一定大于正反应速率
C. ![]() 时,反应达到了化学平衡状态
时,反应达到了化学平衡状态
D. ![]() 时,正反应速率等于逆反应速率
时,正反应速率等于逆反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某试液中只可能含有K+、NH4+、Fe2+、Al3+、Cl-、SO42-、CO32-、AlO2-中的若干种离子,离子浓度均为0.1 mol/L,某同学进行了如下实验,下列说法正确的是

A.原溶液中存在NH4+、Fe2+、Cl-、SO42-
B.滤液X中大量存在的阳离子有NH4+、Fe2+和Ba2+
C.无法确定沉淀C的成分
D.无法确定原试液中是否含有Al3+、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.c(OH-)=1×10-13mol/L的溶液中:Mg2+、K+、SO42-、NO3-
B.![]() =1×10-10的溶液中:Na+、Cu2+、HCO3-、NO3-
=1×10-10的溶液中:Na+、Cu2+、HCO3-、NO3-
C.0. 1 mol·L-1KNO3 溶液:H+、K+、SO42-、I-
D.0. 1 mol·L-1NaHS 溶液: H+、Na+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1843年伦敦泰晤士河隧道终于竣工,英国政界人物在隧道里举行了庆典。但带到隧道的香槟酒没有气泡使庆祝变得索然无味,当庆典过后,走出隧道的人们又有尴尬的事发生了:酒在肚子里发胀,酒气从鼻子、嘴里不断冒出来,有的人穿的马甲被胀开。请回答下列问题:
(1)香槟酒、啤酒、碳酸饮料在开瓶时会观察到有气泡冒出,请你写出与该现象有关的化学平衡方程式:_____。
(2)泰晤士河隧道竣工庆典的尴尬说明_____________________对化学平衡移动存在影响。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T ℃时在2 L的密闭容器中X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,反应温度分别为T1和T2时,Y的体积分数与时间的关系如图2所示。则下列结论正确的是
 A.反应进行的前3 min内,用X表示的反应速率v(X)=0.3 mol·(L·min)-1
A.反应进行的前3 min内,用X表示的反应速率v(X)=0.3 mol·(L·min)-1
B.容器中发生的反应可表示为3X(g)+Y(g) ![]() 2Z(g)
2Z(g)
C.保持其他条件不变,升高温度,反应的化学平衡常数K减小
D.若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制作隐形眼镜的材料应该具有亲水性。聚甲基丙烯酸甲酯(PMMA)是制作隐形眼镜的材料之一。其合成路线如下:
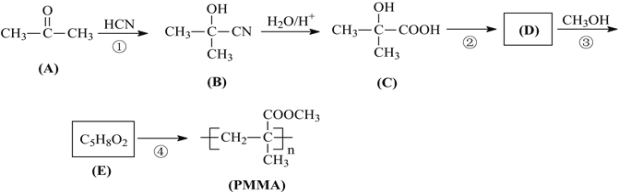
完成下列填空:
(1)写出结构简式:E___;A的一种同分异构体,能与新制氢氧化铜反应,其结构简式为___。
(2)反应①的有机反应类型___。
(3)反应②的试剂和反应条件___。
(4)反应③的化学方程式___。
(5)聚甲基丙烯酸羟乙酯(HEMA)也可制作隐形眼镜(结构简式见图),用HEMA制作的隐形眼镜比PMMA制作的亲水性好,原因是___。
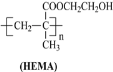
(6)佩戴隐形眼镜最好常滴“人工眼泪”以滋润眼球。有一种“人工眼泪”成分是聚乙烯醇![]() 。已知乙烯醇(CH2=CHOH)不稳定,写出以乙炔为原料(其他无机原料任选)制取聚乙烯醇的合成路线。___。
。已知乙烯醇(CH2=CHOH)不稳定,写出以乙炔为原料(其他无机原料任选)制取聚乙烯醇的合成路线。___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g)===PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
下列说法正确的是
A. 反应在前50 s的平均速率v(PCl3)=0.0032 mol·L-1·s-1
B. 保持其他条件不变,升高温度,平衡时c(PCl3)=0.11 mol·L-1,则反应的ΔH<0
C. 相同温度下,起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3和0.20 mol Cl2,反应达到平衡前v(正)>v(逆)
D. 相同温度下,起始时向容器中充入2.0 mol PCl3和2.0 mol Cl2,达到平衡时,PCl3的转化率小于80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)常温下,有A、B、C、D四种无色溶液,它们分别是![]() 溶液、
溶液、![]() 溶液、盐酸和
溶液、盐酸和![]() 溶液中的一种。已知A、B的水溶液中水的电离程度相同,A、C溶液的pH相同。
溶液中的一种。已知A、B的水溶液中水的电离程度相同,A、C溶液的pH相同。
则:①B是________溶液,C是________。
②常温下若B溶液中![]() 与C溶液中
与C溶液中![]() 相同,B溶液的pH用
相同,B溶液的pH用![]() 表示,C溶液的pH用
表示,C溶液的pH用![]() 表示,则
表示,则![]() ________(填某个数)。
________(填某个数)。
(2)已知某溶液中只存在![]() 四种离子,某同学推测其离子浓度大小顺序可以有以下几种可能:
四种离子,某同学推测其离子浓度大小顺序可以有以下几种可能:
①![]()
②![]()
③![]()
④![]()
则:
(i)上述关系一定不正确的是________(填序号)。
(ii)若溶液中只有一种溶质,则该溶液中离子浓度的大小关系为________(填序号)。
(iii)若四种离子浓度关系有![]() ,则该溶液显________(填“酸性”“碱性”或“中性”)。
,则该溶液显________(填“酸性”“碱性”或“中性”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com