
取一定质量的由两种有机物组成的混合物,无论以何种比例混合,在足量的氧气中充分燃烧后生成的![]() 的物质的量总是相同的,则此混合物是
的物质的量总是相同的,则此混合物是
[
]A
.甲烷和丙烷 B.乙烯和丙烷C
.甲醛和乙酸 D.乙醇和丙醇 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
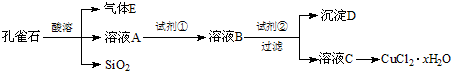
| Fe3+ | Cu2+ | Fe2+ | |
| 开始沉淀的pH | 2.7 | 5.4 | 8.1 |
| 沉淀完全的pH | 3.7 | 6.9 | 9.6 |
| 80a-135b |
| 18b |
| 80a-135b |
| 18b |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 溶解度 温度 化学式 |
0℃ | 10℃ | 20℃ | 30℃ | 40℃ |
| KClO4 | 0.76 | 1.06 | 1.68 | 2.56 | 3.73 |
| KCl | 28 | 31.2 | 34.2 | 37.2 | 40.1 |
| NaClO4 | 167 | 183 | 201 | 222 | 245 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(5分)用实验确定HCOOH是弱电解质。两同学的方案是:
甲:①称取一定质量的HCOOH配制0.1 mol·L-1的溶液100 mL;
②用pH试纸测出该溶液的pH,即可证明HCOOH是弱电解质。
乙:①用已知物质的量浓度的HCOOH溶液、盐酸,分别配制pH=1的两种酸溶液各100 mL;②分别取这两种溶液各10mL,加水稀释为100mL;③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HCOOH是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是 。
(2)甲方案中,说明HCOOH是弱电解质的理由是测得溶液的pH 1(选填>、<、=)。
乙方案中,说明HCOOH是弱电解质的现象是
a.装HCl溶液的试管中放出H2的速率快;
b.装HCOOH溶液的试管中放出H2的速率快;
c.两个试管中产生气体速率一样快:
(3)一定温度下有:a.盐酸;b.硫酸;c.醋酸三种酸。
①当其物质的量浓度相同时,c(H+)由大到小的顺序是___________________________。
②当c(H+)相同、体积相同时,同时加入镁,若产生相同体积的H2(相同状况),则开始时的反应速率____________________。(用a b c的大小关系表示)
查看答案和解析>>
科目:高中化学 来源:2014届河北省高三上学期二调考试化学试卷(解析版) 题型:填空题
Ⅰ.卤化物和卤酸盐在工业生产中有着重要的作用。某小组为探究其中一些盐的性
质,查阅资料并进行实验。查阅资料如下:
① BrO3- + 6I- + 6H+ = 3I2 + Br-+ 3H2O ② 2BrO3- + I2 = 2IO3- + Br2
③ IO3- + 5I- + 6H+ = 3I2 + 3H2O ④ 2IO3- + 10Br-+ 12H+ = I2 + 5Br2 + 6H2O
实验如下:
|
步骤 |
现象 |
|
ⅰ.向盛有30 mL 0.2 mol·L-1 KI溶液的锥形瓶中依次滴入几滴淀粉溶液和足量稀硫酸,再用滴定管逐滴加入KBrO3溶液 |
随着KBrO3溶液滴入,溶液由无色变为蓝色并逐渐加深,最终保持不变 |
|
ⅱ.继续向上述溶液中滴入KBrO3溶液 |
溶液的蓝色逐渐褪去 |
请回答:
(1)根据资料中的反应①~④并结合所学知识,判断IO3-、BrO3-、I2、Br2的氧化性由强到弱的顺序是 ;KBrO3溶液与KBr溶液在酸性条件下反应的离子方程式是 。
(2)若用y表示锥形瓶中含碘物质的物质的量 ,用x表示所滴入KBrO3的物质的量,在下图中画出上述整个实验过程中y随x的变化曲线(要求:在图中标出终点坐标)。

Ⅱ.过碳酸钠中含有少量过氧化钠,甲、乙两位同学各称取一定质量的该样品,并用如下图所示仪器测定样品的纯度。仪器的连接顺序:
甲同学:⑤—⑧—③—⑦—④; 乙同学:⑤—③—②。

已知:过碳酸钠(Na2CO4)、过氧化钠分别跟足量稀硫酸反应的化学方程式如下:
2Na2CO4+2H2SO4=2Na2SO4+2CO2↑+O2↑+2H2O;
2Na2O2+2H2SO4=2Na2SO4+O2↑+2H2O。
(1)甲同学想通过实验测得的数据是____________,他选用的装置________(填序号)是没有必要的。
(2)乙同学想通过实验测得的数据是________________。有人认为按他测得的数据计算出的实验结果可能偏高,原因是________________; 为了测得准确的实验数据,请你将乙同学的实验设计进行改进,写出你所选用仪器的连接顺序(每种仪器最多使用一次,也可以不用):________________(填序号)。
查看答案和解析>>
科目:高中化学 来源:2013届宁夏高二上学期期末考试化学试卷 题型:实验题
(5分)用实验确定HCOOH是弱电解质。两同学的方案是:
甲:①称取一定质量的HCOOH配制0.1 mol·L-1的溶液100 mL;
②用pH试纸测出该溶液的pH,即可证明HCOOH是弱电解质。
乙:①用已知物质的量浓度的HCOOH溶液、盐酸,分别配制pH=1的两种酸溶液各100 mL;②分别取这两种溶液各10 mL,加水稀释为100 mL;③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HCOOH是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是 。
(2)甲方案中,说明HCOOH是弱电解质的理由是测得溶液的pH 1(选填>、<、=)。
乙方案中,说明HCOOH是弱电解质的现象是
a.装HCl溶液的试管中放出H2的速率快;
b.装HCOOH溶液的试管中放出H2的速率快;
c.两个试管中产生气体速率一样快:
(3)一定温度下有:a.盐酸;b.硫酸;c.醋酸三种酸。
①当其物质的量浓度相同时,c(H+)由大到小的顺序是___________________________。
②当c(H+)相同、体积相同时,同时加入镁,若产生相同体积的H2(相同状况),则开始时的反应速率____________________。(用a b c的大小关系表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com