
| A、HClO4、H2SO4、H3PO4的酸性依次减弱 |
| B、HCl、HBr、HI的稳定性依次增强 |
| C、钠、镁、铝的还原性依次减弱 |
| D、P、S、Cl最高正价依次降低 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
A、CO2通入澄清的石灰水中反应的产物: |
B、Fe在Cl2中的燃烧产物: |
C、AlCl3溶液中滴加NaOH后铝的存在形式: |
D、氨水与SO2反应后溶液中的铵盐: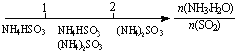 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①和⑤ | B、②和③ |
| C、⑤和⑥ | D、④和⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol任何物质所含有的原子数为NA |
| B、在H2O2+Cl2═2HCl+O2反应中,每生成32g氧气,则转移2NA个电子 |
| C、标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g |
| D、17克氨气所含的电子数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、39K+和40Ca2+微粒中的电子数和中子数都相等 |
| B、D2和He在同温同压时,若体积相等,则质量不相等 |
| C、同一元素的各种同位素的物理性质、化学性质均相同 |
| D、两个质量数和电子数都相等的微粒一定是同种元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、当有0.1mol电子转移时,a极产生1.12L O2(标准状况下) |
| B、b极上发生的电极反应是:4H2O+4e-═2H2↑+4OH- |
| C、c极上发生的电极反应是:O2+4H++4e-═2H2O |
| D、d极上进行还原反应,B中的H+可以通过隔膜进入A |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③⑤②④ |
| B、②①③④⑤ |
| C、②④①③⑤ |
| D、③①②⑤④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子核都是由质子和中子构成的 |
| B、一个氕原子核实际上就是一个质子 |
| C、某原子的相对原子质量就是该原子的质量与一个碳-12原子质量的比值 |
| D、质量数是个化学概念,某元素的质量与该元素的近似相对原子质量在数值上相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com