
| A、C10H9O4 |
| B、C 10H22O3 |
| C、C9H10O4 |
| D、C9H8O4 |
| 该元素相对原子质量×原子数目 |
| 化合物相对分子质量 |
| 180×60% |
| 12 |
| 180×4.4% |
| 1 |
| 180-12×9-8 |
| 16 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
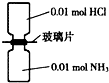 NA表示阿伏加德罗常数的值,常温下,抽去如图所示装置中的玻璃片,使两种气体充分反应.下列说法正确的是( )
NA表示阿伏加德罗常数的值,常温下,抽去如图所示装置中的玻璃片,使两种气体充分反应.下列说法正确的是( )| A、反应前气体的总体积为0.448L |
| B、生成物中含有0.01NA个分子 |
| C、装置中氢元素的总质量为0.04g |
| D、生成物完全溶于水后所得溶液含有0.01NA个NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、浓溴水、NaOH溶液 |
| B、CO2气体、NaOH溶液 |
| C、酒精 |
| D、NaOH溶液、稀HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NO和NO2的密度都比空气大,都可以用向上排空气法收集 |
| B、丙烷和乙醇的分子量相近,二者沸点也相近 |
| C、SO2和CO2都是酸性氧化物,都能与KOH溶液反应 |
| D、Na2O和Na2O2所含元素相同,故与CO2反应产物也相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:3 | B、1:4 |
| C、1:1 | D、3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含有SO42-的溶液:Ca2+、NH4+、HCO3-、Cl- |
| B、c(Fe2+)=0.5 mol/L的溶液:H+、Na+、Cl-、SO42- |
| C、pH=1的溶液:Na+、K+、Cl-、CO32- |
| D、酸性无色透明溶液中:Fe2+、Na+、NO3-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、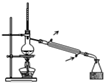 用如图装置可用于分离互不相溶的液体 |
B、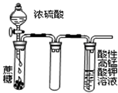 用如图装置酸性KMnO4溶液中没有气泡出现,但溶液颜色会逐渐变浅乃至褪去 |
C、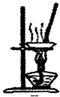 用如图所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
D、 用如图确认CO2和NaOH已发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、1:2 | B、1:1 |
| C、2:5 | D、3:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com