
【题目】0.5mol硝酸铵一定条件下可分解成18g水以及另外一种气态物质,该气态物质可能是
A. NOB. N2OC. N2O3D. N2
【答案】B
【解析】
0.5mol硝酸铵,反应前各种原子的量:1mol N,2mol H,1.5mol O;反应后生成的水中含有的原子:n(H)=2n(H2O)=![]() ×2=2mol ,含有的O原子的物质的量n(O)= n(H2O)=1mol,所以未知气体中含有:N原子为1mol,O原子为0.5mol,不含H原子,据此判断。
×2=2mol ,含有的O原子的物质的量n(O)= n(H2O)=1mol,所以未知气体中含有:N原子为1mol,O原子为0.5mol,不含H原子,据此判断。
18g水的物质的量为n(H2O)=![]() =1mol,反应前0.5mol硝酸铵含有的各种原子的物质的量:N原子0.5mol×2=1mol,H原子0.5mol×4=2mol,O原子0.5mol×3=1.5mol;反应后生成水中含有的原子的物质的量:H原子n(H)=1mol×2=2mol,O原子:n(O)=1mol×1=1mol。因此未知气体中含有:N原子1mol,O原子为1.5mol-1mol=0.5mol,不含H原子;n(N):n(O)=2:1,则未知气体为N2O,故合理选项是B。
=1mol,反应前0.5mol硝酸铵含有的各种原子的物质的量:N原子0.5mol×2=1mol,H原子0.5mol×4=2mol,O原子0.5mol×3=1.5mol;反应后生成水中含有的原子的物质的量:H原子n(H)=1mol×2=2mol,O原子:n(O)=1mol×1=1mol。因此未知气体中含有:N原子1mol,O原子为1.5mol-1mol=0.5mol,不含H原子;n(N):n(O)=2:1,则未知气体为N2O,故合理选项是B。


 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】已知3.6 g碳在6.4 g氧气中燃烧,至反应物耗尽,测得放出热量a kJ。又知12.0 g碳完全燃烧,放出热量为 b kJ。则热化学方程式C(s)+![]() O2(g)===CO(g) ΔH=Q 中Q等于( )
O2(g)===CO(g) ΔH=Q 中Q等于( )
A. -(a-b) kJ·mol-1 B. -(a+b) kJ·mol-1
C. -(5a-0.5b) kJ·mol-1 D. -(10a-b) kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子一定能在指定溶液中大量共存的是
A. pH=l 的溶液中:Ba2+、Fe3+ 、Cl-、SCN-
B. 能使酚酞变红的溶液:Ca2+、K+、HCO3-、CO32-
C.  =10-12的溶液中:NH4+、Cu2+、NO3-、SO42-
=10-12的溶液中:NH4+、Cu2+、NO3-、SO42-
D. 由水电离的c(H+)=10-12mol·L-1的溶液中:Na+、Al3+、Cl-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某可逆反应:2A(g)![]() B(g)+D(g)在密闭固定容积的容器中4种不同条件下进行,B和D的起始浓度均为0,反应物A的浓度随反应时间的变化情况如下表:
B(g)+D(g)在密闭固定容积的容器中4种不同条件下进行,B和D的起始浓度均为0,反应物A的浓度随反应时间的变化情况如下表:
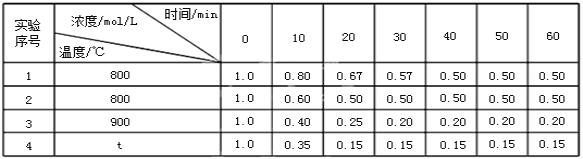
(1)实验1中,在10~20min内,以物质A表示的平均反应速率为_____。
(2)0~20min内,实验2比实验1的反应速率(“快”或“慢”)_____,其原因可能是_____。
(3)实验3比实验1的反应速率(填“快”或“慢”)_____,其原因可能是_____。
(4)从表中可以看出,t_____900(填“>”、“<”、“=”)。
(5)实验3中40分钟时υ(正)_____υ(逆)(填“>”、“<”、“=”)。
(6)实验4中50分钟时B的浓度为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z是周期表中相邻的三种元素。已知X和Y是同主族,Y和Z同周期,它们最外层上的电子数之和为16,则这三种元素可能是
A.Na、K、CaB.N、P、SC.N、P、SiD.F、Cl、S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应C(s)+H2O(g)![]() CO(g)+H2(g)在一个体积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
CO(g)+H2(g)在一个体积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
①增加固体碳的量 ②保持压强不变,充入Ar使体系体积增大
②将容器压缩体积 ④保持体积不变,充入Ar使体系压强增大
A. ①③B. ①④C. ①②D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯度晶体硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场 “革命”。它的制备方法如下图所示,下列说法正确的是
![]()
A. 步骤①的化学方程式为:SiO2+C![]() Si+CO2↑
Si+CO2↑
B. 灼烧熔融的Na2CO3固体,可用石英坩埚
C. 二氧化硅能与氢氟酸反应,而硅不能与氢氟酸反应
D. SiHCl3(沸点33.0℃)中含有少量SiCl4(沸点67.6℃),可通过蒸馏(或分馏)提纯SiHCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将气体A2、B2各1 mol充入1 L的密闭容器中反应,生成气体C,一段时间后,测得c(A2)为0.58 mol·L-1,c(B2)为0.16 mol·L-1,c(C)为0.84 mol·L-1,则C的化学式为( )
A. AB B. A2B C. AB2 D. A2B2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硒(Se)是人体健康必需的一种微量元素。已知Se的原子结构示意图如下,下列说法正确的是
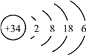
A. 该元素处于第四周期第IVA族B. SeO2既有氧化性又有还原性
C. 该原子的质量数为34D. 酸性:HBrO4 <H2SeO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com