
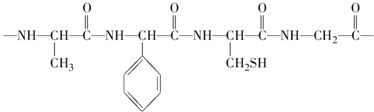
 ,水解需要4个水分子生成氨基酸,水解得到的氨基酸为CH3CH(NH2)COOH、H2NCH2COOH、H2NCH2CH(SH)COOH、H2NCH(C6H5)COOH,以此来解答.
,水解需要4个水分子生成氨基酸,水解得到的氨基酸为CH3CH(NH2)COOH、H2NCH2COOH、H2NCH2CH(SH)COOH、H2NCH(C6H5)COOH,以此来解答. 断碳氮单键,碳上加-OH,氮上加-H,水解得到的氨基酸为CH3CH(NH2)COOH、H2NCH2COOH、H2NCH2CH(SH)COOH、H2NCH(C6H5)COOH,故答案为:CH3CH(NH2)COOH、H2NCH2COOH、H2NCH2CH(SH)COOH、H2NCH(C6H5)COOH;
断碳氮单键,碳上加-OH,氮上加-H,水解得到的氨基酸为CH3CH(NH2)COOH、H2NCH2COOH、H2NCH2CH(SH)COOH、H2NCH(C6H5)COOH,故答案为:CH3CH(NH2)COOH、H2NCH2COOH、H2NCH2CH(SH)COOH、H2NCH(C6H5)COOH; ,H2NCH(C6H5)COOH两分子缩合形成的环状物质,反应为
,H2NCH(C6H5)COOH两分子缩合形成的环状物质,反应为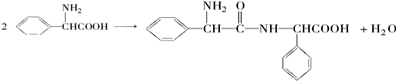 ,
, ;
; ;
; ,水解需要4个水分子生成氨基酸则水解生成的各种氨基酸的式量之和为364+18×4=436,故答案为:436.
,水解需要4个水分子生成氨基酸则水解生成的各种氨基酸的式量之和为364+18×4=436,故答案为:436.


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com