
(1)研究硫及其化合物性质有重要意义。
 硫酸工业生产中涉及如下反应:
硫酸工业生产中涉及如下反应:
2SO2(g)+O2(g) 2SO3(g)。向2L的容器中充入
2SO3(g)。向2L的容器中充入
2molSO2、1molO2,SO2的平衡转化率与温度的关系
如右图所示。
T1温度时反应进行到状态D时,v(正) v(逆)
(填“>”、“<”或“=”)。
温度为T1时,反应的平衡常数K= 。(单位必须写)
若在T3温度时,达平衡时测得反应放出的热量为Q1。此时再向容器中加入2molSO2、1molO2并使之重新达到平衡,测得又放出热量Q2。则下列说法正确的是 。(填字母编号)
a.容器的压强增大原来的两倍 b. Q2一定等于Q1
c. 新平衡时SO2的转化率一定大于80% d. T3时的平衡常数大于T1时的平衡常数
(2)已知:25°C时,Ksp[Mg(OH)2]=5.6×10-12 Ksp(MgF2)=7.4×10-11 。25°C时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+) (填增大、减小或不变);
在等浓度的KOH和KF混合溶液中加入稀MgCl2溶液,首先生成的沉淀是 (写化学式)。
(3)Al2(SO4)3溶液显示酸性,其原因是 (写离子方程式),向某酸化的Al2(SO4)3溶液中加入NaHCO3固体,出现的现象是:有大量气体产生,同时有白色沉淀,试用平衡移动原理解释原因: 。
(4)加热蒸发下列溶液,能析出得到原溶质的是
a. KNO3溶液 b. AlCl3溶液 c. Al2(SO4)3溶液 d.盐酸
(5)25°C时,pH为4的氯化铵溶液和pH为4盐酸溶液中,由水电离出的H+ 浓度之比为 。
 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
某兴趣小组用题图装置探究氨的催化氧化.

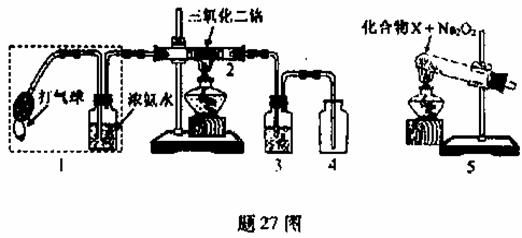
(1)氨催化氧化的化学方程式为___________________.
(2)加热玻璃管2一段时间后,挤压1中打气球鼓入空气,观察到2中物质呈红热状态;停止加热后仍能保持红热,该反应是_________反应(填“吸热”或“放热”).
(3)为保证在装置4中观察到红棕色气体,装置3应装入_________;若取消3,在4中仅观察到大量白烟,原因是___________________.
(4)为实现氨催化氧化,也可用装置5替换装置_________(填装置代号);化合物X为_________(只写一种),Na2O2的作用是___________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
验证淀粉水解可生成还原性糖进行了下列实验,该实验操作步骤的排列顺序正确的是( )
①取少量淀粉加水制成溶液 ②加热煮沸 ③加入新制的Cu(OH)2 悬浊液 ④加几滴稀硫酸 ⑤再加热直至沸腾 ⑥加入碱液,中和直至溶液呈碱性
A.①②④⑤③⑥ B.①④②③⑤⑥ C.①④②⑥③⑤ D.①⑤③④⑥②
查看答案和解析>>
科目:高中化学 来源: 题型:
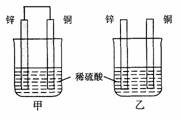
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是
A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的pH均增大
D.产生气泡的速度甲比乙慢
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒温时,一固定容积的容器内发生如下反应:2NH3 (g)  N2 (g)+3H2 (g),达平衡后,再向容器内通入一定量的NH3(g),重新达到平衡后,与第一次平衡时相比,NH3的体积分数( )
N2 (g)+3H2 (g),达平衡后,再向容器内通入一定量的NH3(g),重新达到平衡后,与第一次平衡时相比,NH3的体积分数( )
A.不变 B.增大 C.减小 D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
在通常条件下,下列各组有机物的性质排列错误的是
A.沸点:正戊烷>异戊烷 B.密度:CH3CH2CH2Cl>CH3CH2Cl
C.熔点:CH3CH2CH2Cl>CH3CH2Cl D.水溶性:CH3CH2OH>CH3CH2CH2CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
t ℃时,在体积不变的密闭容器中发生反应:X(g)+3Y(g) 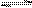 2Z(g),各组分在不同时刻的浓度如下表:
2Z(g),各组分在不同时刻的浓度如下表:
| 物质 | X | Y | Z |
| 初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
| 2 min末浓度/mol·L-1 | 0.08 | a | b |
| 平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法正确的是
A.平衡时,X的转化率为20%
B.t ℃时,该反应的平衡常数为40
C.增大平衡后的体系压强, v正增大,v逆减小,平衡向正反应方向移动
D.前2 min内,用Y的变化量表示的平均反应速率v(Y) = 0.03 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
香豆素是广泛存在于植物中的一类芳香族化合物,大多具有光敏性,有的还具有抗菌和消炎作用。它的核心结构是芳香内酯A,其分子式为C9H6O2。该芳香内酯A经下列步骤转变为水杨酸、乙二酸等物质。
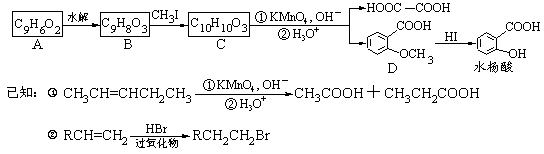
49.写出化合物A的结构简式_____________________。
50.上述转化过程中,属于取代反应的有____个;反应步骤B→C的目的是______________。
51.化合物D有多种同分异构体,其中一类同分异构体是苯的二取代物,且水解后生成的产物之一能发生银镜反应。这类同分异构体(不含C-O-O-结构)共有_____种。
52.鉴别A、B、C三种物质,所需的试剂是________(选填编号)。
a.饱和FeCl3溶液,新制Cu(OH)2悬浊液 b.饱和FeCl3溶液,酸性KMnO4溶液
c.饱和FeCl3溶液,NaOH溶液 d.饱和FeCl3溶液,饱和NaHCO3溶液
53.设计合理方案,由 合成
合成 ,写出相关化学反应流程(无机试剂任取)。
,写出相关化学反应流程(无机试剂任取)。
(用合成路线流程图表示为:A B……
B…… 目标产物)。
目标产物)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中离子一定能够大量共存的是( )
A. 加入Al能放出H2的溶液中:Cl-、SO42-、NO3-、Mg2+
B. 能使淀粉碘化钾试纸显蓝色的溶液中:K+、SO42-、S2-、SO32-
C. c(H+)∶c(OH-)=1∶1012的水溶液中:CO32-、Na+、NO3-、AlO2-
D. 无色溶液中:K+、Na+、MnO4-、SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com