
| A. | 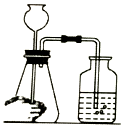 检查装置气密性 | B. | 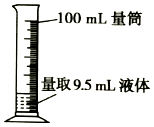 量取 | ||
| C. | 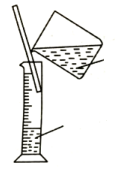 稀释浓硫酸 | D. |  萃取时振荡混合液 |
分析 A.长颈漏斗与大气相连,无法检验装置气密性;
B.量取9.5mL溶液应该选用10mL量筒;
C.不能在量筒中稀释浓硫酸,应该用烧杯;
D.萃取时用左手握住分液漏斗活塞,右手压住分液漏斗口部,把分液漏斗倒转过来振荡,使两种液体充分接触,振荡后打开活塞,将漏斗内气体放出.
解答 解:A.该装置中应该将长颈漏斗换成分液漏斗,否则无法检验装置气密性,故A错误;
B.应该用10mL量筒量筒9.5mL的溶液,否则量取误差较大,故B错误;
C.稀释浓硫酸应该用烧杯,不能在量筒中稀释,故C错误;
D.萃取时振荡混合液,应用左手握住分液漏斗活塞,右手压住分液漏斗口部,把分液漏斗倒转过来振荡,使两种液体充分接触,振荡后打开活塞,将漏斗内气体放出,图示实验操作方法正确,故D正确;
故选D.
点评 本题考查了化学实验方案的评价,题目难度不大,涉及气密性检验、量筒使用、浓硫酸稀释、萃取等知识,明确常见化学实验基本操作方法为解答关键,试题培养了学生的分析能力及化学实验能力.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:实验题
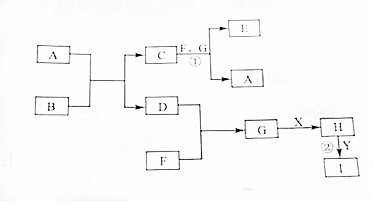 有关物质的转化关系如图所示(部分物质与条件已略去).其中A,D,F,G为常见的气体,D为单质,A,F,G为氧化物,G为棕红色;B为淡黄色固体.X是最常见的液体,Y是常见的金属单质,I溶液为蓝色,
有关物质的转化关系如图所示(部分物质与条件已略去).其中A,D,F,G为常见的气体,D为单质,A,F,G为氧化物,G为棕红色;B为淡黄色固体.X是最常见的液体,Y是常见的金属单质,I溶液为蓝色, .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H1=△H2=△H3 | B. | △H2<△H1<△H3 | C. | △H2=△H3>△H1 | D. | △H2=△H3<△H1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯不与溴水反应,但苯能从溴水中提取溴单质 | |
| B. | 苯在一定条件下能发生加成反应和取代反应,但不能发生氧化反应 | |
| C. | 苯和乙烯都能使酸性KMnO4溶液褪色 | |
| D. | 苯在一定条件下与氢气、硝酸等发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t/min | 2 | 3 | 7 | 9 |
| n(Y)mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 反应前 2 min 的平均速率 v(Z)=2.0×10-3 mol/(L•min) | |
| B. | 其他条件不变,降低温度,反应达到新平衡前 v(逆)>v(正) | |
| C. | 该温度下此反应的平衡常数 K=1.44 | |
| D. | 其他条件不变,再充入 0.2 mol Z,平衡时 X 的体积分数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同温同压下,含有相同分子数的两种气体,占有相同的体积 | |
| B. | 同温同压下,相同物质的量的两种任何气体,含有相同的分子数 | |
| C. | 同温同压下,相同体积的两种气体,物质的量相同 | |
| D. | 同温同压下,2升O2与2升由CO2和CO组成的混合气体含有相同的原子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,NA个CCl4分子所占的体积为22.4 L | |
| B. | 常温常压下,18 g H2O中含有的原子总数为3NA | |
| C. | 标准状况下,2.24 L SO3中含有的分子数目为0.1NA | |
| D. | 常温常压下,2.24 L CO和CO2混合气体中含有的碳原子数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.9gNa2O2固体中含有的阴离子数为0.05 NA | |
| B. | 标准状况下,2.24LCCl4所含原子数为0.5 NA | |
| C. | 1L 0.1mol/L醋酸溶液中含有的CH3COOH分子数为0.1 NA | |
| D. | 56g铁丝与一定量Cl2发生反应,当铁粉反应完全时,电子转移的数目可能为2.2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.56L | B. | 1.68L | C. | 2.24L | D. | 1.12L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com