
| A. | 1:2 | B. | 2:3 | C. | 3:2 | D. | 1:1 |
分析 等质量的铝粉,分别与等体积的氢氧化钠溶液和硫酸恰好完全反应,由2Al+2NaOH+2H2O=2NaAlO2+3H2↑、2Al+3H2SO4=Al2(SO4)3+3H2↑可得2Al~2NaOH~3H2SO4~3H2,则n(NaOH):n(H2SO4)=2:3,体积相等时,两溶液溶液的物质的量浓度之比等于物质的量之比.
解答 解:等质量的铝粉,分别与等体积的氢氧化钠溶液和硫酸恰好完全反应,说明参加反应的铝的物质的量相等.
由2Al+2NaOH+2H2O=2NaAlO2+3H2↑、2Al+3H2SO4=Al2(SO4)3+3H2↑可知:当参加反应的铝的物质的量相等时,放出氢气的体积相等,n(NaOH):n(H2SO4)=2:3,由于氢氧化钠溶液和稀硫酸体积相同,故3c(NaOH)=2c(H2SO4),即c(NaOH):c(H2SO4)=2:3,
故选:B.
点评 本题考查铝的性质,根据化学方程式找出2Al~2NaOH~3H2SO4~3H2比例关系是解题的关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
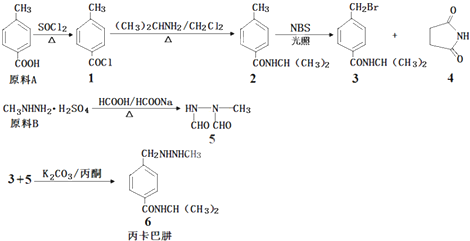
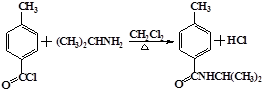 .
.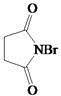 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “春蚕到死丝方尽,蜡烛成灰泪始干”中的“丝”、“泪”分别是纤维素和油脂 | |
| B. | 乙醇、金属钠和乙酸分别属于非电解质、非电解质和弱电解质 | |
| C. | Na2O2、Al2O3、C4H10分别属于碱性氧化物、两性氧化物和离子化合物 | |
| D. | 煤的气化、石油的分馏分别是化学变化、物理变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
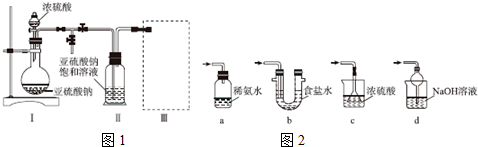

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,23g乙醇和甲酸的混合物中含有O-H键的数目为0.5NA | |
| B. | 40g SiC中含有Si-C键的数目为2NA | |
| C. | 标准状况下,22.4L乙醛含有分子的数目为NA | |
| D. | 2mol亚油酸(9,12-十八碳二烯酸,C17H31COOH)中含有双键的数目是4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 断开1mol AB(g)分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为A-B键的键能.下表列出了一些化学键的键能E:
断开1mol AB(g)分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为A-B键的键能.下表列出了一些化学键的键能E:| 化学键 | H-H | Cl-Cl | O═O | C-Cl | C-H | O-H | H-Cl |
| E/kJ•mol-1 | 436 | 247 | x | 330 | 413 | 463 | 431 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com