
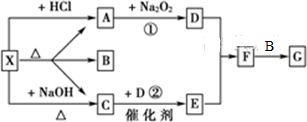
| ||
| △ |
| ||
| △ |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、“新物质”就是自然界中不存在的物质 |
| B、“新物质”就是与变化前的物质在颜色、状态等方面有所不同的物质 |
| C、“新物质”就是与变化前的物质在元素组成上不同的物质 |
| D、“新物质”就是在组成或结构上与变化前的物质不同的物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 化学键的键能是原子间形成1mol化学键(或其逆过程)时释放(或吸收)的能量.以下是部分共价键键能的数据:H-S:364kJ?mol-1,S-S:266kJ?mol-1,S═O:522kJ?mol-1,H-O:464kJ?mol-1.
化学键的键能是原子间形成1mol化学键(或其逆过程)时释放(或吸收)的能量.以下是部分共价键键能的数据:H-S:364kJ?mol-1,S-S:266kJ?mol-1,S═O:522kJ?mol-1,H-O:464kJ?mol-1.查看答案和解析>>
科目:高中化学 来源: 题型:
A、 制取并收集乙炔 |
B、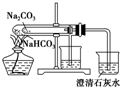 比较NaHCO3,Na2CO3的热稳定性 |
C、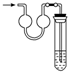 吸收HCl气体且防止倒吸 |
D、 实验室中制取少量乙酸乙酯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com