
下列叙述错误的是( )
A.合金材料中可能含有非金属元素
B.人造纤维、合成纤维和光导纤维都是有机高分子化合物
C.植物的光合作用是地球上规模最大的化学反应,它把太阳光能变成化学能
D.在汽车排气管上加装“催化转化器”是为了减少有害气体的排放
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
对可逆反应4NH3(g)+5O2(g)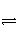
 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )
A.达到化学平衡时,4v正(O2)=5v逆(NO)
B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D.化学反应速率关系是2v正(NH3)=3v正(H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
对牛奶中的蛋白质进行下列实验:取30.0 mL牛奶,用盖尔达法分离蛋白质,把氮完全转化为氨,用50.0 mL 0.5 mol·L-1 H2SO4溶液吸收后,剩余的酸用1 mol·L-1 NaOH溶液中和,需38.0 mL。
(1)30.0 mL牛奶中含有多少克氮?
(2)如果蛋白质中含氮16%(质量分数),计算牛奶中含蛋白质的质量分数。(已知牛奶的密度是1.03 g·mL-1)
提示:盖尔达法:蛋白质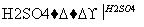 硫酸铵
硫酸铵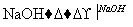 氨
氨
查看答案和解析>>
科目:高中化学 来源: 题型:
有以下一系列反应,最终产物是乙二酸:
A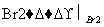 B
B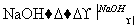 C
C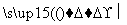 D
D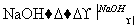 E
E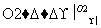 F
F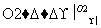 HOOC—COOH
HOOC—COOH
已知B的相对分子质量比A大79。
(1)推测C、F的结构简式:C__________,F__________。
(2)B→C的反应类型是____________________。
(3)C→D的化学方程式:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学在资源利用、环境保护等与社会可持续发展密切相关的领域发挥着积极作用。下列做法与社会可持续发展理念相违背的是( )
A.改进汽车尾气净化技术,减少大气污染物的排放
B.开发利用可再生能源,减少化石燃料的使用
C.研发可降解高分子材料,减少“白色污染”
D.过度开发矿物资源,促进地方经济发展
查看答案和解析>>
科目:高中化学 来源: 题型:
保护环境是每一个公民的责任。下列做法:
①推广使用无磷洗涤剂,②城市生活垃圾分类处理,③推广使用一次性木质筷子,④推广使用清洁能源,⑤过量使用化肥、农药,⑥推广使用无氟冰箱。其中有利于保护环境的是( )
A.①②④⑤ B.②③④⑥
C.①②④⑥ D.③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
人们对酸碱的认识已有几百年的历史,经历了一个由浅入深、由低级到高级的认识过程。我们目前中学课本中的酸碱理论是1887年阿伦尼乌斯(Arrhenius)提出的电离理论。
探究过程:
(1)1905年富兰克林(Franklin)深入研究了水和液氨的相似性,把阿伦尼乌斯以水为溶剂的个别现象推广到任何溶液,提出了酸碱溶剂理论。溶剂理论认为凡能离解而产生溶剂正离子的物质为酸,凡能离解而产生溶剂负离子的物质为碱。试写出液氨弱电离的方程式(生成的两种微粒电子数相等):________________________________________________________________________。
(2)1923年丹麦化学家布朗斯特(Bronsted)和英国化学家劳莱(Lowry)提出了质子论。凡是能够释放质子(氢离子)的任何含氢原子的分子或离子都是酸;凡是能与质子(氢离子)结合的分子或离子都是碱。按质子理论:下列微粒在水溶液中既可看作酸又可看作碱的是________。
A.H2O B.NH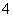 C.OH- D.HCO
C.OH- D.HCO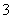 E.CH3COO- F.Cl-
E.CH3COO- F.Cl-
(3)1923年路易斯(Lewis)提出了广义的酸碱概念。凡是能给出电子对而用来形成化学键的物质是碱;凡是能和电子对结合的物质都是酸。如:
酸(电子对接受体) 碱(电子对给予体) 反应产物
H+ + - —→ H:OH
试指出下列两个反应中的酸或碱:
①H3BO3+H2OH++B(OH)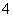 该反应中的碱是________;
该反应中的碱是________;
②NaH+H2O===NaOH+H2↑ 该反应中的酸是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应合乎实际并用于工业生产的是( )
A.Na在Cl2中燃烧制NaCl B.高温分解石灰石制生石灰
C.Cl2与石灰水作用制漂白粉 D.H2与Cl2充分混合点燃制HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
操作1:将1 L 1.00 mol·L-1的Na2CO3溶液逐滴加入到1 L 1.25 mol·L-1的盐酸中;操作2:将1 L 1.25 mol·L-1的盐酸逐滴加入1 L 1.00 mol·L-1 的Na2CO3溶液中,两次操作产生的气体体积之比(同温同压下)是
A.5∶2 B.2∶5 C.1∶1 D.2∶1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com