
分析 设在容积为2.0L的密闭容器中充入0.60mol N2(g)和1.60mol H2(g),反应在一定条件下达到平衡时,设转化的氮气为xmol,则
N2(g)+3H2(g)?2NH3(g)
开始 0.60 1.60 0
转化 x 3x 2x
平衡 0.60-x 1.60-3x 2x
NH3的物质的量分数为$\frac{4}{7}$,则$\frac{2x}{0.60-x+1.60-3x+2x}$=$\frac{4}{7}$,
解得x=0.04mol,
结合转化率=$\frac{转化的量}{开始的量}$×100%、K为生成物浓度幂之积与反应物浓度幂之积的比、互为相反的两个反应的K互为倒数关系来计算..
解答 解:设在容积为2.0L的密闭容器中充入0.60mol N2(g)和1.60mol H2(g),反应在一定条件下达到平衡时,设转化的氮气为xmol,则
N2(g)+3H2(g)?2NH3(g)
开始 0.60 1.60 0
转化 x 3x 2x
平衡 0.60-x 1.60-3x 2x
NH3的物质的量分数为$\frac{4}{7}$,则$\frac{2x}{0.60-x+1.60-3x+2x}$=$\frac{4}{7}$,
解得x=0.4mol,
①该条件下N2的平衡转化率为$\frac{0.40mol}{0.60mol}$×100%=66.7%,
答:N2的平衡转化率为66.7%;
②N2(g)+3H2(g)?2NH3(g)的K=$\frac{(\frac{0.80mol}{2L})^{2}}{(\frac{0.4mol}{2L})^{3}×(\frac{0.2mol}{2L})}$=200,则该条件下反应2NH3(g)═N2(g)+3H2(g)的平衡常数为$\frac{1}{200}$=0.005,
答:2NH3(g)?N2(g)+3H2(g)的平衡常数为0.005.
点评 本题考查化学平衡的计算,为高频考点,把握化学平衡三段法、转化率及K的计算为解答的关键,侧重分析与计算能力的考查,注意物质的量分数的计算方法,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 由反应①可推知:CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(l),△H>-574 kJ•mol-1 | |
| B. | 反应①②转移的电子数不相同 | |
| C. | 若用标准状况下4.48L CH4 还原NO2至N2,放出的热量为173.4kJ | |
| D. | 若用标准状况下4.48L CH4 还原NO2至N2,整个过程中转移的电子总数为0.8mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
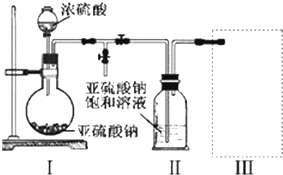
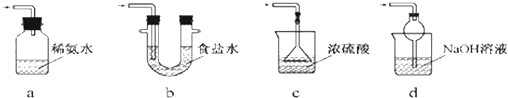

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 化学键 | C-C | C-H | H-H | C-O | C=O | H-O |
| 键能/kJ•mol-1 | 348 | 413 | 436 | 358 | 750 | 463 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| t/(℃) | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
 如图是金属钨晶体中的一个晶胞的结构示意图,它是一种体心立方结构.实验测得金属钨的密度为19.30g•cm-3,钨的相对原子质量是183.9.假设金属钨原子为等径刚性球,试完成下列问题:
如图是金属钨晶体中的一个晶胞的结构示意图,它是一种体心立方结构.实验测得金属钨的密度为19.30g•cm-3,钨的相对原子质量是183.9.假设金属钨原子为等径刚性球,试完成下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
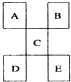
| A. | D一定足金属元素,其金属性比C强 | |
| B. | C的最高价氧化物水化物显强酸性 | |
| C. | E的原子序数一定是A的5倍,且原予半径比A大 | |
| D. | B的氢化物是以分子形式存在,且分子间存在氢键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com