
| A.依据相对分子质量的数据,推测乙醇和丙烷沸点的相对高低 |
| B.依据溶解度的数据,选择用重结晶的方法可将粗苯甲酸提纯 |
| C.依据沸点的数据,判断用分馏的方法从石油中获取汽油和煤油等 |
| D.依据燃烧热的数据、热化学方程式和盖斯定律,可计算一些反应的反应热 |
科目:高中化学 来源:不详 题型:计算题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.碳和一氧化碳 |
| B.1g碳和2mol碳 |
| C.淀粉和纤维素 |
| D.3mol乙炔(C2H2)和1mol苯(C6H6) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.如图条件下实验过程中没有热量损失 |
| B.若改用60ml0.50mol/L盐酸跟50ml0.55mol/L的NaOH溶液进行反应,通过测定反应过程中所放出的热量相等 |
| C.图中实验装置缺少环形玻璃搅拌棒 |
| D.烧杯间填满碎纸条的作用是固定小烧杯。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氢原子的能量比氢分子的能量低 |
| B.两个氢原子结合成一个氢分子时放出435.7kJ能量 |
| C.1mol氢分子分解成2mol氢原子要吸收435.7kJ能量 |
| D.2mol氢原子结合1mol氢分子成要吸收435.7kJ能量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.物质发生化学变化都伴随着能量变化 |
| B.任何反应中的能量变化都表现为热量变化 |
| C.物质变化时若伴有能量变化,则一定是化学变化 |
| D.没有物质的化学变化,也就没有能量的变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
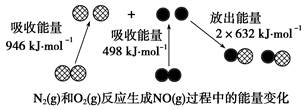
| A.1 mol N2(g)和1 mol O2(g)反应放出的能量为180 kJ |
| B.1 mol N2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的总能量 |
| C.通常情况下,N2(g)和O2(g)混合能直接生成NO |
| D.NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题


 N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 升温至t2
升温至t2 时,溶质的质量分数B>A
时,溶质的质量分数B>A查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2 mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。
AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2 mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com