
正确掌握化学基本概念和化学用语是学好化学的基础,下列有关表述中正确的是
A.过氧化氢与过氧化钠中含有化学键的类型完全相同
B.NaHSO4在水溶液中的电离方程式为:NaHSO4=Na++H++SO42-
C.因为NH4HCO3是强电解质,所以在其水溶液中只存在水解平衡,不存在电离平衡
D.H216O、D216O、H218O、D218O互为同素异形体
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016届广东省高三第一次月考理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.摩尔是用来衡量微观粒子多少的一种物理量
B.在一定的温度和压强下,各种气体的摩尔体积相等
C.阿伏加德罗常数的数值是0.012 kg 14C所含的原子个数
D.若气体摩尔体积为22.4 L•mol﹣1,则所处条件为标准状况
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三上学期开学考试化学试卷(解析版) 题型:选择题
A、B、C、D、E五种短周期主族元素,它们的原子序数依次增大。已知:A和C、B和D分别位于同主族,且B、D质子数之和是A、C质子数之和的2倍。下列说法正确的是
A.原子半径的大小顺序:r(B)>r(C)>r(D)
B.C的最高价氧化物对应水化物的碱性在同周期中最强
C.E分别与A、C形成的化合物中化学键类型相同
D.B的简单气态氢化物的热稳定性比D的弱
查看答案和解析>>
科目:高中化学 来源:2016届山东省枣庄市高三9月阶段性学情检测化学试卷(解析版) 题型:选择题
标准状况下V L氨气溶解在1 L水中(水的密度近似为1 g·mL-1),所得溶液的密度为ρ g·mL-1,质量分数为w,物质的量浓度为c mol·L-1,则下列关系中不正确的是
A.ρ= B.w=
B.w=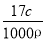
C.w=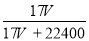 D.c=
D.c=
查看答案和解析>>
科目:高中化学 来源:2016届山东省新高三开学初模拟检测化学试卷(解析版) 题型:选择题
下列电离方程式中,错误的是
A.H2CO3  H++HCO3- ; HCO3-
H++HCO3- ; HCO3-  H++CO32-
H++CO32-
B.H2SO4 == 2H++SO42-
C.NaHS == Na++H++S2-
D.CH3COOH  H+ + CH3COO―
H+ + CH3COO―
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列物质转化在给定条件下能实现的是
①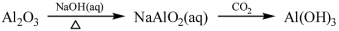
②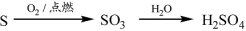
③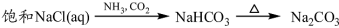
④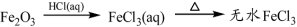
⑤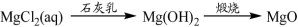
A.①③⑤ B.②③④ C.②④⑤ D.①④⑤
查看答案和解析>>
科目:高中化学 来源:2016届湖北省黄石市高三9月调研考试化学试卷(解析版) 题型:填空题
(13分)节能减排已经成为全社会的共识,浙江省在原先推行乙醇汽油的基础上,开始试点甲醇汽油(即在汽油中添加一定量的甲醇),根据检测的数据分析认为,若宁波全市的140余万辆机动车全部使用甲醇汽油,一年内能减少有害气体(一氧化碳)排放将近100万吨。甲醇常利用煤气化过程中生成的CO和H2来制备:CO+2H2 CH3OH。请根据图示回答下列:
CH3OH。请根据图示回答下列:
(1)关于该反应的下列说法中,正确的是 (填字母):
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
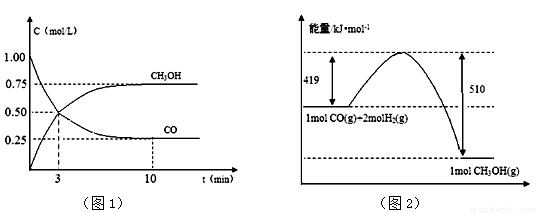
(2)现进行如下实验,在体积为1L的密闭容器中,充入1molCO和3molH2,净测得CO和CH3OH(g)的浓度随时间变化如(图1)所示。从反应开始到平衡,CO的平均反应速率v(CO)= ,该反应的平衡常数K= 。
(3)恒容条件下,达到平衡后,下列措施中能使n(CH3OH)/n(CO)增大的有 。
A.升高温度 B.充入He气
C.再充入1molCO和3molH2 D.使用催化剂
(4)若在一体积可变的密闭容器中充入1molCO、2molH2和1molCH3OH,达到平衡时测的混合气体的密度是同温同压下起始的1.6倍(此过程三种物质均处于气态),则平衡时混合气体的平均摩尔质量=_____g/mol。
(5)根据(图2),写出此反应的热化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2016届重庆市高三7月月考化学试卷(解析版) 题型:选择题
NA为阿伏加德罗常数,下述正确的是
A.58.5g氯化钠晶体中含有NA个氯化钠分子
B.20g重水(D2O)中含有的电子数为10NA
C.标准状况下,22.4LCCl4含有NA个CCl4分子
D.120gNaHSO4晶体中阳离子和阴离子的总数为3NA
查看答案和解析>>
科目:高中化学 来源:2016届河南省郑州市新高三年级调研检测化学试卷(解析版) 题型:填空题
A.【化学—选修3.物质结构与性质】(15分)周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族,e的最外层只有1个电子,但次外层有18个电子。请填写下列空白。
(1)e元素基态原子的核外电子排布式为_____________。
(2)b、c、d三种元素的第一电离能数值由小到大的顺序为___________(填元素符号),其原因是____________。
(3)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为___________________;分子中既含有极性共价键,又含有非极性共价键的化合物是______________(填化学式,写出两种)。
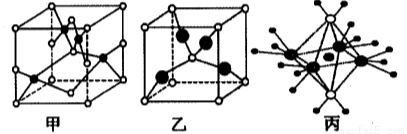
(4)已知c、e能形成晶胞如图甲和图乙所示的两种化合物,化合物的化学式为分别为:甲________________,乙___________;甲高温易转化为乙的原因是______________。
(5)这5种元素形成的一种1 :1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构(如图丙所示)。该化合物中,阴离子为_______________,该化合物加热时首先失去的组分是______________,判断理由是________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com