
分析 Ⅰ.(1)由题意可知,CuH是氢化亚铜,据化合物中化合价代数和等于0判断;
(2)根据“在新制Cu(OH)2浊液中滴入N2H4•H2O水溶液,同时产生无色无味的气体”判断反应物、生成物,然后写出反应的化学方程式;
(3)据CuH与过量稀硫酸反应的离子方程式计算.
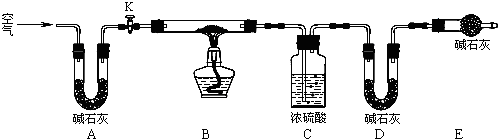
Ⅱ.(1)依据实验步骤和目的分析,步骤4是反应完毕后,需要继续通空气,让装置冷却;
(2)装置E的作用是防止空气中的二氧化碳和水蒸气进入D装置;
(3)根据化学方程式找出与x、y有关的物质质量,对比分析,碱式碳酸铜分解的化学方程xCu(OH)2•yCuCO3$\frac{\underline{\;\;△\;\;}}{\;}$(x+y)CuO+xH2O+yCO2↑要测定x/y,可以测定生成的水和二氧化碳的质量,即测定C装置增重的质量和D装置增重的质量或BC、BD装置质量计算判断;根据计算结果写出该样品组成的化学式.
解答 解:Ⅰ.(1)CuH是氢化亚铜,据化合物中化合价代数和等于0可知,H为-1价,故答案为:-1;
(2)在新制Cu(OH)2浊液中滴入N2H4•H2O水溶液,产生无色无味的气体,根据化合价变化,铜离子化合价降低被还原,能够被氧化生成无色无味的气体可能为N、O元素,由于氧气具有氧化性,不可能生成氧化亚铜,所以该气体只能是氮气,根据化合价升降法配平,反应的化学方程式为:4Cu(OH)2+N2H4•H2O═2Cu2O+N2↑+7H2O,
故答案为:4Cu(OH)2+N2H4•H2O═2Cu2O+N2↑+7H2O;
(3)CuH与过量稀硫酸反应的离子方程式为2CuH+2H+=Cu+Cu2++H2↑,生成$\frac{6.72L}{22.4L/mol}$=0.3mol氢气时,参加反应的氢离子物质的量为0.3mol,所以硫酸的物质的量为0.15mol,
故答案为:0.15mol;
Ⅱ.(1)步骤4反应完毕后,需要继续通空气,让装置冷却,所以步骤4为:打开K1,继续通一段时间空气至装置冷却,
故答案为:打开K1,继续通一段时间空气至装置冷却;
(2)装置E的作用是防止空气中的二氧化碳和水蒸气进入D装置,D装置是吸收生成的二氧化碳的,C装置是吸收生成的水的,如果没有装置E,会使D装置质量增重偏大,即生成的二氧化碳质量偏大,则$\frac{x}{y}$的值会偏小
故答案为:偏小;
(3)碱式碳酸铜分解的化学方程xCu(OH)2•yCuCO3$\frac{\underline{\;\;△\;\;}}{\;}$(x+y)CuO+xH2O+yCO2↑要测定x/y的值,可以测定生成的水和二氧化碳的质量,即测定C装置增重的质量和D装置增重的质量,故可选CD,
xCu(OH)2•yCuCO3$\frac{\underline{\;\;△\;\;}}{\;}$(x+y)CuO+xH2O+yCO2↑
18x 44y
2.25g 5.5g
则:$\frac{18x}{2.25g}$=$\frac{44y}{5.5g}$,解得:$\frac{x}{y}$=1:1;
若测出反应后玻璃管中样品的质量以及装置C增重的质量,即已知方程式中氧化铜和水的质量关系,可求出$\frac{x}{y}$的值,故可选BC,
xCu(OH)2•yCuCO3$\frac{\underline{\;\;△\;\;}}{\;}$(x+y)CuO+xH2O+yCO2↑
(x+y)×80 18x
20g 2.25g
则:$\frac{(x-y)×80}{20g}$=$\frac{18x}{2.25g}$,解得:$\frac{x}{y}$=1:1;
同样若已知反应后玻璃管中样品的质量以及装置C增重的质量,即已知方程式中氧化铜和二氧化碳的质量关系,可求出$\frac{x}{y}$的值.故可选BD,
xCu(OH)2•yCuCO3$\frac{\underline{\;\;△\;\;}}{\;}$(x+y)CuO+xH2O+yCO2↑
(x+y)×80 44y
20g 5.5g
则:$\frac{(x-y)×80}{20g}$=$\frac{44y}{5.5g}$,解得$\frac{x}{y}$=1:1;
根据以上计算结果可知该样品组成的化学式为:Cu(OH)2•CuCO3,
故答案为:BC、BD、CD;Cu(OH)2•CuCO3.
点评 本题考查了化合价计算、离子方程式书写以及据化学方程式的计算、物质组成的测量方法,题目难度中等,明确浓硫酸增重的质量是生成的水的质量、碱石灰增重的质量是生成的二氧化碳的质量为解答关键,试题侧重考查学生的分析、理解能力及化学计算、化学实验能力.


 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:解答题
| 弱酸 | 电离平衡常数(25℃) |
| HClO | K=2.98×10-8 |
| H2CO3 | K1=4.3×10-7 K2=5.6×10-11 |
| H2SO3 | K1=1.54×10-2 K2=1.02×10-7 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | KOH | B. | Na2CO3 | C. | HClO4 | D. | MgSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol水蒸汽 | B. | 标准状况下1 mol CCl4 | ||
| C. | 标准状况下44 g二氧化碳 | D. | 0℃、202 kPa时2 g氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2通过Na2O2使其增重b g时,反应中转移电子数为bNA/44 | |
| B. | 18 g D2O中含有质子的数目为NA | |
| C. | 12 g C3H6 与 16 g C2H4的混合物完全燃烧,可生成CO2分子数为2 NA | |
| D. | 0.1 mol AlCl3完全水解转化为氢氧化铝胶体,生成 0.1 NA个胶粒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X与Y能形成两种常见的气态化合物 | |
| B. | 原子半径的大小顺序:r(Z)>r(R)>r(X)>r(Y) | |
| C. | X、Z分别与R形成的化合物中化学键类型不同 | |
| D. | 含有Y、Z、R三种元素的化合物最多只有2种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 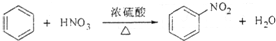 | |
| B. |  | |
| C. | CH3CH2OH+CH3COOH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O | |
| D. | CH4+Cl2$\stackrel{光照}{?}$CH3Cl+HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用磨口玻璃瓶、玻璃塞保存NaOH溶液 | |
| B. | 加入适量的金属钠除去酒精中少量的水 | |
| C. | 分液时,分液漏斗中的上层液体应由上口倒出 | |
| D. | 能使湿润的淀粉碘化钾试纸变蓝色的气体一定是Cl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com