
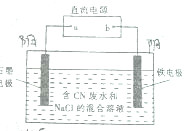
 工业上,在强碱性条件下用电解法除去废水中的CN-,装制如图所示,依次发生的反应有:
工业上,在强碱性条件下用电解法除去废水中的CN-,装制如图所示,依次发生的反应有:| A. | a是电源的正极 | |
| B. | 铁电极上发生的电极反应式为2H++2e-═H2↑ | |
| C. | 为了使电解池连续工作,需要不断补充NaOH | |
| D. | 除去1mol CN-,电解过程中共产生标准状况下11.2L气体 |
分析 根据发生的电极反应,可以知道金属铁是阴极,石墨电极是阳极,根据电解质中离子的放电顺序以及电极反应和电子的转移知识来回答即可.
解答 解:A、金属铁是阴极,石墨电极是阳极,与a相连的为石墨电极,所以a是电源的正极,故A正确;
B、金属铁是阴极,为溶液中的氢离子得电子发生还原反应,电极反应式为2H++2e-═H2↑,故B正确;
C、根据电极反应的离子,为了使电解池连续工作,需要补充氢氧化钠,故C正确;
D、根据反应:3Cl2+2CNO-+8OH-═N2+6Cl-+2CO32-+4H2O,除去1mol CN-,消耗1.5mol氯气,生成0.5mol氮气,所以电解过程中共产生标准状况下(1.5+0.5)×22.4=44.8L气体,故D错误.
故选D.
点评 本题考查学生电解池的工作原理以及电极反应式等,注意把握电解池的工作原理,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 用食盐腌制食物 | B. | 用盐酸除去铁钉表面的铁锈 | ||
| C. | 用液氨作制冷剂 | D. | 用漂粉精消毒游泳池中的水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | υ(A)=0.20mol/(L•min) | B. | υ(B)=0.45 mol/(L•min) | ||
| C. | υ(C)=0.30 mol/(L•min) | D. | υ(D)=0.35 mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室制溴苯时,将苯与液溴混合后加到有铁丝的反应容器中 | |
| B. | 实验室制硝基苯时,将硝酸与苯混合后再滴加浓硫酸 | |
| C. | 实验时手指上不小心沾上苯酚,立即用70℃以上的热水清洗 | |
| D. | 苯中含苯酚杂质,除去杂质的方法:加入溴水,过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径大小:Na>S>O | B. | 稳定性:HI>HBr>HCl>HF | ||
| C. | 碱性强弱:KOH>Ca(0H)2>Mg(OH)2 | D. | 还原性强弱:I一>CI一>F? |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
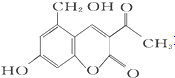 M(假蜜环菌素)
M(假蜜环菌素)| A. | M的分子式为C12H10O5 | |
| B. | 1 mol M最多可和6mol H2发生加成反应 | |
| C. | M可发生水解反应 | |
| D. | M可与 HBr反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最终三支试管的颜色各不相同 | |
| B. | A试管中Fe(OH)3含量最高 | |
| C. | 直接加热蒸发Fe2(SO4)3溶液可得到Fe2(SO4)3晶体 | |
| D. | B试管中Fe2(SO4)3不能发生水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜矿石在细菌作用下直接转换为单质铜,这个过程中叫做生物炼铜 | |
| B. | 人们通常用标准燃烧热或热值来衡量燃料燃烧放出热量的大小,相同条件下,某物质的热值越高,其标准燃烧越大 | |
| C. | 铅蓄电池是最常见的二次电池,可根据硫酸的密度来判断铅蓄电池是否需要充电 | |
| D. | “地沟油”禁止食用,但可以通过物理变化制肥皂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com