
��12�֣�Ǧ�����ǵ��͵Ŀɳ��͵�أ���������������Ƕ��Բ��ϣ�����ܷ�ӦʽΪ��
Pb+PbO2+4H++2SO42- 2PbSO4+2H2O
2PbSO4+2H2O
��ش��������⣨�������⡢����������ԭ����
��1���ŵ�ʱ�������ĵ缫��Ӧʽ��________________�����Һ��H2SO4��Ũ�Ƚ���________�������·ͨ��1 mol����ʱ�������ϸ��������������________g
��2������ȫ�ŵ�ľ�PbO2��Pbʱ������ͼ����
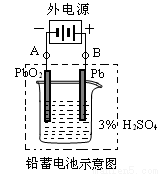
����һ��ʱ�����A�缫������________��B�缫������________����ʱǦ���ص��������ļ��Խ�________
 ��˼ά������ҵ���ټ��ִ�ѧ������ϵ�д�
��˼ά������ҵ���ټ��ִ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016�캣��ʡ����У���˸�����һ��������ѧ���������棩 ���ͣ�ѡ����
һ�������£���ѧ��ѧ�������ʼס���֮���������ת����ϵ�����ҿ�����
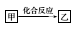
A��Al(OH)3 B��H2SO4 C��MgCl2 D��CuS
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��������������ʵ����ѧ��һ�����л�ѧ���������棩 ���ͣ�ѡ����
���ж����ӵ����ɼ����۵����ⲻ��ȷ���ǣ� ��
A��ͬ��ͬѹ�£���������֮�ȵ������ǵ����ʵ���֮��
B��ͬ��ͬѹ�£���������֮�ȵ������ǵ�����֮��
C��ͬ��ͬѹ�£���ͬ��������������ȵ������ǵ���Է�������֮��
D��ͬ�µ����£������ѹǿ֮�ȵ������ǵ����ʵ���֮��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���㽭��Ҧ��ѧ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����л����������ȷ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ�߶������п��Ի�ѧ�Ծ��������棩 ���ͣ������
��ѧ�ڿɳ�����չ����Դ���ۺ����������˾��ס�ú��ʯ�͡���Ȼ����Щ��ʯ��Դ��θ��õ��ۺ����ã���ؼ���������죬��ش��������⣺
��1����ˮú������Ҫ��ѧ��Ӧ����ʽΪ��C(s)+H2O(g) 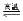 CO(g)+H2(g)���˷�Ӧ�����ȷ�Ӧ
CO(g)+H2(g)���˷�Ӧ�����ȷ�Ӧ
�ٴ˷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪ ��
������������̼��ת���ʵĴ�ʩ�� ������д��Ӧ��ĸ��
A������C��s�� B������H2O��g�� C�������¶� D������ѹǿ
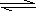 ��2���ϳ����ϳɼ״�����Ҫ��Ӧ�ǣ�2H2(g)+CO(g) CH3OH(g) ��H=��90.8kJ�� mol��1
��2���ϳ����ϳɼ״�����Ҫ��Ӧ�ǣ�2H2(g)+CO(g) CH3OH(g) ��H=��90.8kJ�� mol��1
T���´˷�Ӧ��ƽ�ⳣ��Ϊ160�����¶��£���2L�ܱ������п�ʼֻ����CO��H2����Ӧ10min���ø���ֵ����ʵ������£�
���� | H2 | CO | CH3OH |
���ʵ�����mol�� | 0.4 | 0.2 | 0.8 |
�ٸ�ʱ����ڷ�Ӧ����v(H2)= mol��L��1��min��1��
�ڱȽϴ�ʱ�����淴Ӧ���ʵĴ�С��v(��)_______v(��)�����������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ����ׯ���и߶�10��ѧ����黯ѧ���������棩 ���ͣ�ѡ����
����˵����ȷ����
A��ͬ��ͬѹ�£�H2 (g)+Cl2(g)= 2HCl(g)�ڹ��պ͵�ȼ�����µġ�H��ͬ
B���κ��������кͷ�Ӧ����1 mol H2O�Ĺ����У������仯����ͬ
C����֪����2H2(g) +O2(g) =2H2O(g) ��H=-a kJ��mol-1,
��2H2(g)+O2 (g)= 2H2O��1�� ��H=-b kJ��mol-1����a>b
D����֪����C(s��ʯī)+O2 (g)=CO2(g) ��H=- 393.5kJ��mol-1��
��C(s�����ʯ)+O2(g)=CO2 (g) ��H=- 395.0 kJ��mol-1
��C(s��ʯī)=C(s�����ʯ) ��H= -1.5 kJ��mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭���߰���ѧ��һ�����л�ѧ�����ص�ࣩ�������棩 ���ͣ�ʵ����
ʵ����������0.5mol��L-1��NaOH��Һ500mL�����������������ձ��� 100mL��Ͳ ��100mL����ƿ�ܽ�ͷ�ιܢݲ�������������ƽ�������룩��ҩ��
��1������ʱ������ʹ�õ�������____________������ţ�����ȱ�ٵ�������___________����ʵ���������õ��������������÷ֱ���_________________��__________________��
��2��������Һʱ��һ����Է�Ϊ���¼������裺 �ٳ����ڼ��� ���ܽ� �ܵ�תҡ�Ȣ�ת�Ƣ�ϴ�Ӣ߶��ݢ���ȴ������ȷ�IJ���˳��Ϊ__________________________���������գ��������ڢٲ����������NaOH______________g��
��3�����в��������ʹ��Һ�����ʵ���Ũ��ƫ�͵��� _________ ��
A��û�н�ϴ��Һת������ƿ��
B������ʱ�������������
C������ʱ����������ƿ�Ŀ̶���
D�����ݺ���ҡ�ȡ����ã�����Һ����ڿ̶��ߣ��ټ�����ˮ�����̶�
��4����ijѧ����������ƽ����ҩƷʱ����������ƽ���̷���20g���룬��ƽ��ƽ��ʱ�����λ����ͼ�����ͬѧ������ҩƷ��ʵ������Ϊ_________g��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ������и�һ�ϵ��Ĵ��¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
ijЩ������ˮ�п��ܺ����������ࡣ������������������ˮʱ������ˮ�ĵط����ɻҺ�ɫ���ݴ˿����жϴ˵ص�ˮ�к��У� ��
A������ B������ C������ D������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ����������������и߶������в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����Ȼ�ѧ����ʽ��д��ȷ����(��H�ľ���ֵ����ȷ)
A��C2H5OH(l)��3O2(g)==2CO2(g)��3H2O(g) ��H����1367.0 kJ/mol(ȼ����)
B��NaOH(aq)��HCl(aq)==NaCl(aq)��H2O(l) ��H����57.3 kJ/mol(���)
C��S(s)��O2(g)==2SO2(g) ��H����296.8 kJ/mol(��Ӧ��)
D��2NO2==O2��2NO ��H����116.2 kJ/mol(��Ӧ��)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com