
【题目】向FeCl3、Al2(SO4)3的混和溶液中逐滴加入Ba(OH)2溶液,形成沉淀的情况如下图所示。Fe(OH)3、Al(OH)3沉淀的生成与溶解的pH列于下表。(已知:偏铝酸钡易溶于水)。以下推断正确的是
氢氧化物 | 溶液pH | |||
开始沉淀 | 完全沉淀 | 沉淀开始溶解 | 沉淀完全溶解 | |
Fe(OH)3 | 2.3 | 3.1 | — | — |
Al(OH)3 | 3.3 | 5.2 | 7.8 | 12.8 |

A. OA段产生的沉淀为:Fe(OH)3和Al(OH)3
B. AB段可能发生的反应是:Al3++3OH-=Al(OH)3↓
C. Al3+的物质的量浓度是2mol·L-1
D. C点沉淀的质量为806g
【答案】B
【解析】向含Al2(SO4)3 和 FeCl3的混合溶液与Ba(OH)2 溶液反应的实质是Fe3+,Al3+与OH-、Ba2+与SO42-之间的离子反应,如下:Ba2++SO42-═BaSO4↓,Fe3++3OH-=Fe(OH)3 ↓,Al3++3OH-═Al(OH)3 ↓,Al(OH)3 +OH-═AlO2-+2H2O,假设1molAl2(SO4)3 中SO42-完全被沉淀所需Ba(OH)2 量为3mol,提供6molOH-,图表分析铁离子先沉淀,由图象分析,OA段为加入3molBa(OH)2 ,发生反应Ba2++SO42-═BaSO4↓,得到3molBaSO4沉淀,C点为氢氧化铝溶解后的沉淀物质的量为氢氧化铁和硫酸钡沉淀共5mol,所以氢氧化铁沉淀为2mol,氢氧化铝沉淀为2mol;分析判断OA段沉淀3mol钡离子,1mol铁离子和1mol铝离子;AB段为沉淀1mol铁离子,1mol铝离子;BC段为溶解氢氧化铝消耗氢氧化钡1mol;
A、OA段可能发生的反应有沉淀钡离子,铁离子,铝离子,反应为,3Ba2++6OH-+3SO42-+Al3++Fe3+→3BaSO4↓+Fe(OH)3 ↓+Al(OH)3 ↓,也可能发生3Ba2++6OH-+3SO42-+2Fe3+→3BaSO4↓+2Fe(OH)3 ↓,故A错误;B、AB段可能发生的反应是Al3++3OH-→Al(OH)3 ↓,故B正确;C、由BC线段,Al3+ ~Al(OH)3 ~AlO2―~OH― ,Ba(OH)2 1mol,含2molOH― ,Al3+ 物质的量为2mol,无体积,故C错误;D、C点为氢氧化铝溶解后的沉淀物质的量为氢氧化铁和硫酸钡沉淀共5mol,所以氢氧化铁沉淀为2mol,BaSO4为3mol,沉淀共233g/mol×3mol+107g/mol×2mol=913g,故D错误;故选B。


科目:高中化学 来源: 题型:
【题目】某小组同学做“硫在氧气中燃烧”的实验时,老师建议在集气瓶底部放少量NaOH溶液吸收生成的SO2。这种做法引起了同学们的思考:SO2与NaOH是否发生反应。
【查阅资料】通常状况下,1体积水约能溶解40体积SO2。
【实验方案】同学们向充满SO2的软塑料瓶中迅速倒入一定量NaOH溶液,拧紧瓶盖,振荡,发现塑
料瓶变瘪,他们认为SO2与NaOH发生了反应。
【反思与改进】甲同学认为上述实验不够严谨,理由是_________________。于是同学们设计了如下两
个改进方案。
方案一:
实验操作 | 实验现象 |
向两个充满SO2的200 mL软塑料瓶中分别注入10 mL水和NaOH溶液,振荡,对比。 | 两个瓶子变瘪的程度完全相同 |
乙同学认为由于两个瓶子变瘪的程度完全相同,因此无法证明SO2与NaOH是否发生了反应。试分析导致两个瓶子变瘪的程度完全相同的原因是_____________________。他认为若改变注入水和NaOH溶液的体积便可达到实验目的,注入液体的体积可以是__________(填序号)。
a.15 mL b.8 mL c.5 mL d.3 mL
方案二:
实验操作 | 实验现象 |
利用如图所示装置进行实验: 向两个充满SO2的300 mL集气瓶 中分别加入6 mL水和NaOH溶液, 一段时间后,打开止水夹,对比。
| 倒吸入两个集气瓶中的液体体积完全相同 |
丙同学认为上述方案也无法证明SO2与NaOH是否发生反应。你认为导致吸入液体的体积完全相同的原因是___________________。
丁同学思考后,将上述装置进行了改进,便达到实验目的。改进装置如下图所示,你认为装置B的作用是_______________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】日本福岛核电站泄漏的核燃料衰变产物有放射性元素![]() 、
、![]() 等,其中
等,其中![]() 是个双刃剑,医院可以用它来治疗甲状腺癌;但是如果没有癌症,它也可能诱发甲状腺癌。下列有关说法中不正确的是
是个双刃剑,医院可以用它来治疗甲状腺癌;但是如果没有癌症,它也可能诱发甲状腺癌。下列有关说法中不正确的是
A. 碘131I原子核所含中子数是78
B. 核能的利用证实原子的可分性
C. 碘127I原子和放射性碘原子131I属于同位素
D. 碘127I原子和碘131I原子的质子数不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列影响化学反应速率的外界因素中,肯定能使化学反应速率加快的方法是( )
①升高温度 ②加入正催化剂 ③增大反应物浓度 ④将块状固体反应物磨成粉末 ⑤增大压强
A.①②③⑤ B.①②④⑤ C.①③④⑤ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】建构数学模型来研究化学问题,既直观又简洁。下列建构的数轴模型正确的是
A. 钠在氧气中燃烧后得到的氧化产物:![]()
B. 铁在Cl2中燃烧后得到的氧化产物:![]()
C. FeBr2溶液中通入Cl2,铁元素存在形式:![]()
D. NH3与Cl2反应,反应产物:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有48.4 g碱式碳酸镁样品(化学式:xMgCO3·yMg(OH)2·zH2O,x、y、z为正整数),将其分为二等份,一份样品充分灼烧至恒重进行热重分析,结果如图所示。另一份投入150 mL某浓度的盐酸中,充分反应后生成CO2 4.48 L(已折算成标准状况下),所得溶液稀释至250 mL,测得溶液的c(H+)=0.100 mol·L-1。
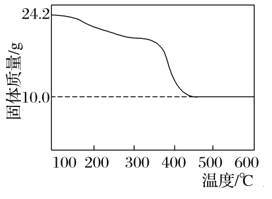
按要求回答下列问题:
(1)盐酸的物质的量浓度c(HCl)=________mol·L-1。
(2)x∶y∶z=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】清初《泉州府志》物产条载:“初,人不知盖泥法,元时南安有黄长者为宅煮糖,宅垣忽坏,去土而糖白,后人遂效之。”文中“盖泥法”的原理与下列相同的是( )
A. 活性炭净水 B. 用漂白粉漂白织物
C. 除去KNO3中的NaCl D. 除去河水中泥沙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1mol任何微粒所含的微粒数约为6.02×1023,在1L 1mol/L的CaCl2溶液中,所含Ca2+数约为
A. 1 B. 2 C. 6.02×1023 D. 1.204×1024
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关系正确的是( )
A. 密度:CCl4>CHCl3>H2O
B. 熔点:2,3一二甲基丁烷>2一甲基丁烷>戊烷
C. 同质量的物质完全燃烧耗O2量:乙烯>乙炔>甲烷
D. 同物质的量物质完全燃烧耗O2量:环已烷>苯>苯甲酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com