
| A. | 水结成冰 | B. | 干冰气化 | C. | 食盐溶于水 | D. | 浓硫酸稀释 |
科目:高中化学 来源: 题型:选择题
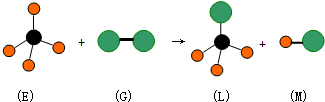
| A. | 反应过程中E中共价键断裂,G中共价键保持不动 | |
| B. | E中存在非极性键 | |
| C. | M分子有可能是HCl | |
| D. | 上述反应的类型是加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
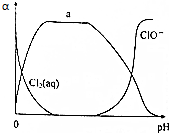 氯及其化合物在自来水消毒和果蔬保鲜等方面应用广泛.
氯及其化合物在自来水消毒和果蔬保鲜等方面应用广泛.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 保持容器容积不变,向其加入1molH2(g),反应速率一定加快 | |
| B. | 保持容器容积不变,向其中加入1molN2(N2不参加反应),反应速率一定加快 | |
| C. | 保持容器内气体压强不变,向其中加入1molN2(N2不参加反应),反应速率一定加快 | |
| D. | 保持容器内气体压强不变,向其中加入1molH2(g)和1molI2(g),反应速率一定加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常作为气体的干燥剂 | B. | 常温下不能与铁发生反应 | ||
| C. | 滴在蔗糖上,蔗糖会变黑 | D. | 工业上主要采用接触法制备 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2的摩尔质量是64 g | |
| B. | 标准状况下18 g水的体积是22.4 L | |
| C. | 在标准状况下,20 mL NH3 与60 mL O2所含的分子数比为1:3 | |
| D. | 1mol/LMgCl2溶液中含有Cl-的数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn | B. | Fe | C. | Al | D. | Mg |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
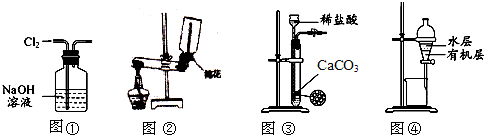
| A. | 用图①所示装置除去Cl2中含有的少量HCl | |
| B. | 用图②所示装置制备并收集O2 | |
| C. | 用图③所示装置制取少量的CO2气体 | |
| D. | 用图④所示装置分离汽油萃取碘水后已分层的有机层和水层 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com