
| m |
| M |
| 0.9g |
| 90g/mol |


科目:高中化学 来源: 题型:
| A、水的摩尔质量是18g |
| B、2mol水的摩尔质量是1mol水摩尔质量的2倍 |
| C、任何物质的摩尔质量都就是它的相对分子质量或相对原子质量 |
| D、水的摩尔质量是氢气摩尔质量的9倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)已知常温下pH=2的高碘酸(H3IO5)溶液与pH=12的NaOH溶液等体积混合,所得混合溶液呈酸性;0.01mol/L的碘酸(HIO3)溶液与pH=12的NaOH溶液等体积混合,所得混合溶液呈中性.请回答下列问题:
(1)已知常温下pH=2的高碘酸(H3IO5)溶液与pH=12的NaOH溶液等体积混合,所得混合溶液呈酸性;0.01mol/L的碘酸(HIO3)溶液与pH=12的NaOH溶液等体积混合,所得混合溶液呈中性.请回答下列问题:| c(H+) |
| c(CH3COOH) |
| c(OH-) |
| c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
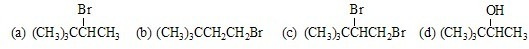
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、22.4L氩气和1mol氢气 |
| B、2g氢气和16g氧气 |
| C、同温同压下,2L氢气和2L水 |
| D、常温常压下1mol氧气和标准状况下2g氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AlCl3 |
| B、FeCl3 |
| C、BaCl2 |
| D、AgNO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com