
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.0.1 mol/L的NaOH溶液:K+、AlO2-、SO42-、CO32-
B.0.1 mol/LFeCl3溶液:K+、NH4+、I-、SCN-
C.0.1 mol/L的Na2CO3溶液:K+、Ba2+、NO3-、Cl-
D.c(H+)/c(OH-)=1×1014的溶液:Ca2+、Na+、I-、NO3-
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2013-2014黑龙江省高二下学期期末考试化学试卷(解析版) 题型:推断题
(12分)某些有机化合物之间具有如下转化关系:
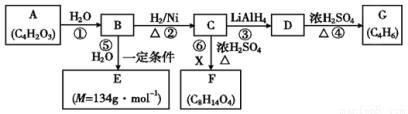
其中:A是一种五元环状化合物,其分子中只有一种化学环境的氢原子;F核磁共振氢谱显示有三种不同化学环境的氢原子,且峰面积之比为2∶2∶3;G是合成顺丁橡胶的主要原料。
已知:① 
 2RCOOH(其中R是烃基)
2RCOOH(其中R是烃基)
②R—COOH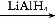 R—CH2OH(其中R是烃基)
R—CH2OH(其中R是烃基)
(1)A的结构简式是 。
(2)B中所含官能团的名称是 。
(3)写出反应类型:③ ,④ 。
(4)⑥的化学方程式为 。
(5)E的结构简式: 。有机物Y与E互为同分异构体,且具有相同的官能团种类和数目,则Y的结构简式可能有 种。
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高一下学期期末考试化学试卷(解析版) 题型:选择题
近期《美国化学会志》报道,中国科学家以二氧化碳为碳源,金属钠为还原剂,在470℃、80MPa下合成出金刚石,具有深远意义。下列说法不正确的是( )
A.由二氧化碳合成金刚石是化学变化 B.金刚石是碳的一种同位素
C.钠被氧化最终生成碳酸钠 D.金刚石中只含有非极性共价键
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高三终极预测理综化学试卷(解析版) 题型:选择题
下图为雾霾的主要成分示意图。下列说法不正确的是
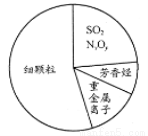
A.重金属离子可导致蛋白质变性
B.苯是最简单的芳香烃
C.SO2和NxOy都属于酸性氧化物
D.汽车尾气的大量排放是造成雾霾天气的人为因素之一
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高三第三次模拟考试理综化学试卷(解析版) 题型:选择题
在特制的密闭真空容器中加入一定量纯净的氨基甲酸铵固体(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:
NH2COONH4(s)  2NH3(g)+CO2(g),已知15℃时,平衡气体总浓度为2.4×10-3mol/L,下列说法中正确的是
2NH3(g)+CO2(g),已知15℃时,平衡气体总浓度为2.4×10-3mol/L,下列说法中正确的是
A.密闭容器中气体的平均相对分子质量不变则该反应达到平衡状态
B.15℃时氨基甲酸铵的分解平衡常数为2.048×10-9(mol/L)3
C.恒温下压缩体积,NH3的体积分数减小
D.再加入一定量氨基甲酸铵,可加快反应速率
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高二下学期期末考试化学试卷(解析版) 题型:填空题
[物质结构与性质](15分)
下表为长式周期表的一部分,其中的序号代表对应的元素。
① |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ② |
|
|
|
|
|
|
|
|
|
|
| ③ | ④ | ⑤ | ⑥ |
|
| ⑦ |
|
|
|
|
|
|
|
|
|
|
|
|
|
| ⑧ |
|
|
|
|
|
| ⑨ |
|
|
|
| ⑩ |
|
|
|
|
|
|
|
(1)写出上表中元素⑨原子的外围电子排布式__________。
(2)在元素③与①形成的水果催熟剂气体化合物中,元素③的杂化方式为__________杂化;元素⑦与⑧形成的化合物的晶体类型是__________。
(3)元素④的第一电离能__________元素⑤(填写“>”“=”或“<”)的第一电离能;元素④与元素①形成的最简单的X分子的空间构型为__________。请写出与元素④的单质互为等电子体分子、离子的化学式__________(各写一种)。
(4)在测定元素①与⑥形成化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是_______。
(5)元素④的最高价氧化物对应的水化物稀溶液与元素⑦的单质反应时,元素④被还原到最低价,该反应的化学方程式为__________。
(6)将过量的X通入含有元素⑩的蓝色硫酸盐溶液中,反应的离子方程式为__________;元素⑩的某种氧化物的晶体结构如图所示,其中实心球表示元素⑩原子,则一个晶胞中所包含的氧原子数目为__________。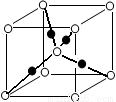
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高二下学期期末考试化学试卷(解析版) 题型:选择题
火法炼铜首先要焙烧黄铜矿,反应为:CuFeS2+O2 Cu2S+FeS+SO2 则下列说法正确的是
Cu2S+FeS+SO2 则下列说法正确的是
A.CuFeS2既是氧化剂又是还原剂,硫元素既被氧化又被还原 B.每生成1molSO2转移6mol电子
C.SO2既是氧化产物又是还原产物,FeS只是还原产物 D.每转移1.2 mol电子,有0.3 mol氧气被还原
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高一下学期期末考试化学试卷(解析版) 题型:实验题
(5分)哈三中某化学课外学习小组利用图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去)。请填空:
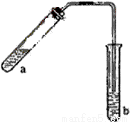
①试管a中需加入浓硫酸、冰醋酸和乙醇各2mL,正确的加入顺序是 。
②为防止a中的液体在实验时发生暴沸,在加热前应采取的措施是 。
③试管b中加有饱和Na2CO3溶液,其作用是 。
④反应结束后,振荡试管b,静置。观察到的现象是 。
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高二下学期期末考试化学试卷(解析版) 题型:选择题
MnO2的一些性质或用途如图,下列说法正确的是 ( )
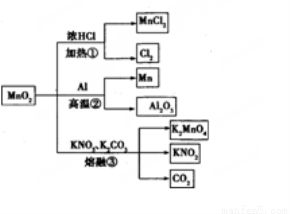
A.①、②、③三个反应中MnO2均作氧化剂
B.足量MnO2与2 L 10 mol/LHCl共热,可生成5 mol C12
C.反应②若生成1 mol Al2O3,则反应过程中转移12 mol电子
D.反应③中K2CO3和KNO3的化学计量数均为1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com