
分析 电解质在水溶液中或熔融状态下能够导电的化合物;非电解质在熔融状态和水溶液中都不能导电的化合物;
在水溶液中完全电离的是强电解质,部分电离的是弱电解质,据此分析.
解答 解:①H2O部分电离,是弱电解质;
②石墨是单质,既不是电解质也不是非电解质;
③NH4NO3在水溶液中完全电离,是强电解质;
④AgCl在熔融状态下能完全电离,故为电解质,且为强电解质;
⑤CH3COOH在水溶液中部分电离,是弱电解质;
⑥硫酸在水溶液中完全电离,是强电解质;
⑦NH3•H2O在水溶液中能部分电离,是电解质且为弱电解质;
⑧蔗糖在熔融状态和水溶液中都不能导电,是非电解质;
故为强电解质的是③④⑥,弱电解质为①⑤⑦,非电解质的为⑧.
故答案为:③④⑥;①⑤⑦;⑧.
点评 本题考查强弱电解质、非电解质概念的辨析,以及杂质的去除,难度中等.要注意除杂时,不能引入新的杂质.


科目:高中化学 来源: 题型:选择题
| A. | HCl+NaOH═NaCl+H2O | B. | SO3+H2O═H2SO4 | ||
| C. | 2Na+Cl2$\frac{\underline{\;点燃\;}}{\;}$2NaCl | D. | CaCO3$\frac{\underline{\;高温\;}}{\;}$ CaO+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
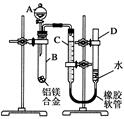 某学习小组用如图所示装置测定铝镁合金中铝的质量分数和铝的相对原子质量.
某学习小组用如图所示装置测定铝镁合金中铝的质量分数和铝的相对原子质量.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠与盐酸;氢氧化铜与盐酸 | B. | BaCl2与Na2SO4;Ba(OH)2与H2SO4 | ||
| C. | Na2CO3与硝酸;CaCO3与硝酸 | D. | 石灰石与硝酸反应;石灰石与盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的Na2CO3和NaHCO3分别与足量盐酸反应,NaHCO3产生的CO2多 | |
| B. | 等物质的量的盐酸分别与足量的Na2CO3和NaHCO3反应,Na2CO3产生的CO2多 | |
| C. | 相同温度在水中的溶解度:Na2CO3大于NaHCO3 | |
| D. | 等物质的量的Na2CO3和NaHCO3分别与足量的盐酸反应,消耗盐酸的量一样多 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
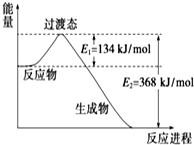 (1)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234KJ/mol.
(1)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234KJ/mol.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2CO (g )+O2(g )═2CO2 (g )△H=-556kJ•mol-1 | |
| B. | CH4(g )+2O2 (g )═CO2(g )+2H2O (l )△H=-890kJ•mol-1 | |
| C. | 2H2(g )+O2(g )═2H2O(l )△H=-571.6kJ•mol-1 | |
| D. | H2(g )+Cl2 (g )═2HCl (g)△H=-184.6kJ•mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com