
科目:高中化学 来源:2016-2017学年吉林省高二上9月月考化学卷(解析版) 题型:选择题
下列各式中不正确的是
A.HF+H2O H3O++F-
H3O++F-
B.NaHCO3=Na++HCO3-,HCO3- H++CO32-
H++CO32-
C.Ag2S(s) 2Ag+(aq)+ S2-(aq)
2Ag+(aq)+ S2-(aq)
D.S2-+2H2O H2S +2OH-
H2S +2OH-
查看答案和解析>>
科目:高中化学 来源:2017届海南中学高三上第二次月考化学试卷(解析版) 题型:填空题
0.1 mol的镁、铝混合物溶于100 mL 2 moI/LH2SO4溶液中,然后再滴加l mol/LNaOH溶液。请回答:
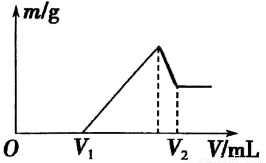
(l)若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示。当V1=160mL时,则金属粉末中n(Mg)=_________ mol,V2=________mL。
(2)若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)=________mL。
(3)若混合物仍为0.1 mol,其中Mg粉的物质的量分数为a,用100 mL2mol/L1硫酸溶解此混合物后,再加入450 mL l moI/LNaOH溶液,所得沉淀中无A1(OH)3。满足条件的a的取值范围是__________。
查看答案和解析>>
科目:高中化学 来源:2017届吉林省高三上学期9月月考化学试卷(解析版) 题型:填空题
离子推断题:有一未知的无色溶液,可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Fe3+、Al3+,NO3-、CO32-、SO42-,现取两份100mL溶液进行如下实验:
①第一份加入足量的BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,称量沉淀质量为6.99g;
②第二份逐滴滴加NaOH溶液,测得沉淀的物质的量与NaOH溶液的体积关系如下图所示。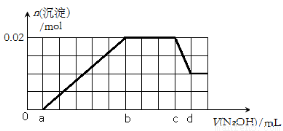
根据上述实验事实,回答以下问题:
⑴该溶液中一定不存在的阳离子有 ;
⑵在实验②中,NaOH溶液滴至b~c段过程中发生的离子反应方程式为 ;NaOH溶液的浓度为 (用含字母c、d的代数式表示);
⑶确定原溶液一定含有Mg2+、Al3+、H+,其物质的量之比n(Mg2+): n(Al3+):n(H+)为 (填数字,下同);
⑷原溶液中NO3-的浓度为c(NO3-),则c(NO3-)的取值范围为 。
查看答案和解析>>
科目:高中化学 来源:2017届吉林省高三上学期9月月考化学试卷(解析版) 题型:选择题
下列指定反应的离子方程式正确的是
A.将铜丝插入稀硝酸中:Cu+4H++2NO3- Cu2++2NO2↑+H2O
Cu2++2NO2↑+H2O
B.向Fe2(SO4)3溶液中加入过量铁粉:Fe3++Fe 2Fe2+
2Fe2+
C.向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3·H2O Al(OH)3↓+3NH4+
Al(OH)3↓+3NH4+
D.向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+  H2SiO3↓+2Na+
H2SiO3↓+2Na+
查看答案和解析>>
科目:高中化学 来源:2017届湖南省邵阳市高三上第一次月考化学试卷(解析版) 题型:推断题
顺丁橡胶、制备醇酸树脂的原料M以及杀菌剂N的合成路线如下:

 ⅰ
ⅰ
ⅱ.RCH===CHR′ RCHO+R′CHO(R,R′代表烃基或氢)
RCHO+R′CHO(R,R′代表烃基或氢)
(1)CH2===CH—CH===CH2的名称是 。
(2)反应Ⅰ的反应类型是(选填字母)___________。a.加聚反应 b.缩聚反应
(3)顺式聚合物P的结构式是(选填字母)___________。

(4)A的相对分子质量为108。
①反应Ⅱ的化学方程式是 。
②1 mol B完全转化成M所消耗的H2的质量是________g。
(5)反应Ⅲ的化学方程式是 。
(6)A的某些同分异构体在相同的反应条件下也能生成B和C,写出其中一种同分异构体的结构简式 。
查看答案和解析>>
科目:高中化学 来源:2017届湖南省邵阳市高三上第一次月考化学试卷(解析版) 题型:选择题
下列说法正确的是 ( )
A.乳酸薄荷醇酯( )仅能发生水解、氧化、消去反应
)仅能发生水解、氧化、消去反应
B.乙醛和丙烯醛( )不是同系物,它们与氢气充分反应后的产物也不是同系物
)不是同系物,它们与氢气充分反应后的产物也不是同系物
C.淀粉和纤维素在酸催化下完全水解后的产物都是葡萄糖
D.CH3COOCH2CH3与CH3CH2COOCH3互为同分异构体,1H—NMR谱显示两者均有三种不同的
氢原子且三种氢原子的比例相同,故不能用1H—NMR来鉴别
查看答案和解析>>
科目:高中化学 来源:2017届湖北省高三上学期调研测试化学试卷(解析版) 题型:实验题
某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液。在FeCl2溶液中需加入少量铁屑,其目的是____________________。
(2)甲组同学取2mLFeCl2溶液.加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为_________________________。
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和l滴KSCN溶液,溶液变红,煤油的作用是_______________。
(4)丙组同学取10 mL0.1mol/LKI溶液,加入6mL0.1mol/LFeCl3溶液混合。分别取2mL此溶液于3 支试管中进行如下实验:
①第一支试管中加入1mLCCl4充分振荡、静置,CCl4层呈紫色;
②第二只试管中加入1滴K3[Fe(CN)6] 溶液,生成蓝色沉淀;
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是__________(填离子符号);实验①和③说明:在I-过量的情况下,溶液中仍含有______(填离子符号),由此可以证明该氧化还原反应为_______________。
(5)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为_______________________;一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成。产生气泡的原因是_____________;生成沉淀的原因是_________________(用平衡移动原理解释)。
查看答案和解析>>
科目:高中化学 来源:2017届湖北省高三上学期9月月考化学试卷(解析版) 题型:填空题
在日常生活中,为了达到更好的清洁效果,经常有人会将洁厕液(含有盐酸)与84消毒液混合使用,从而会发生引发中毒的事故。
(1)两种日化产品主要成分中都含有氯元素,该元素在元素周期表中位置是 。
(2)84消毒液的主要成分是次氯酸钠,写出次氯酸钠的电子式: 。
(3)常温下,0.1mol/L的NaClO溶液的PH=9.7,原因 。常温下HClO的电离平衡常数为 。洁厕液与84消毒液混合后会生成有毒的氯气。写出该反应的离子方程式 。
(4)高铁酸钾是一种高效多功能水处理剂,工业上常采用NaClO氧化法生产,反应原理为:
①在碱性条件下,利用NaClO氧化硝酸铁,制得Na2FeO4,该反应的离子反应方程式为 。
②Na2FeO4与KOH反应生成K2FeO4:Na2FeO4+2KOH=K2FeO4+2NaOH;K2FeO4在水溶液中易水【解析】
4FeO42-+10H2O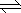 4Fe(OH)3+8OH-+3O2,在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用 溶液(填序号)
4Fe(OH)3+8OH-+3O2,在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用 溶液(填序号)
a.水 b.NH4Cl、异丙醇 c.Fe(NO3)3、异丙醇 d.CH3COONa、异丙醇
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com