
【题目】CO2与H2的混合气体5g,在150℃时和足量的氧气混合,用电火花充分引燃,在相同状况下再将反应后所得混合气体通入到足量的Na2O2中,测得Na2O2固体增重的质量为3.4g,则原混合气体中CO2的质量分数为( )
A. 25% B. 75% C. 88% D. 32%
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是
A.在0.1 mol NaHSO4晶体中阳离子与阴离子总数为0.3NA
B.25℃时,pH=13的1.0 LBa(0H)2溶液中含有的OH-数目为0.2NA
C.常温常压下,4.4gCO2和N2O混合物中所含有的原子数为0.3 NA
D.1L1 mol·L-1FeCl3完全水解生成NA个胶体粒子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为FeO·Cr2O3,还含有硅、铝等杂质。制备流程如图所示:
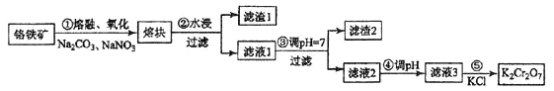
回答下列问题:
(1)步骤①的主要反应为:FeO·Cr2O3+Na2CO3+NaNO3![]() Na2CrO4+ Fe2O3+CO2+ NaNO2
Na2CrO4+ Fe2O3+CO2+ NaNO2
上述反应配平后FeO·Cr2O3与NaNO3的系数比为__________。该步骤不能使用陶瓷容器,原因是________________。
(2)滤渣1中含量最多的金属元素是____________,滤渣2的主要成分是_____________及含硅杂质。
(3)步骤④调滤液2的pH使之变____________(填“大”或“小”),原因是___________________(用离子方程式表示)。
(4)有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,蒸发浓缩,冷却结晶,过滤得到K2Cr2O7固体。冷却到___________(填标号)得到的K2Cr2O7固体产品最多。

a.80℃ b.60℃ c.40℃ d.10℃
步骤⑤的反应类型是___________________。
(5)某工厂用m1 kg 铬铁矿粉(含Cr2O3 40%)制备K2Cr2O7,最终得到产品 m2 kg,产率为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】主族元素A,B,C,D的原子序数都小于18,A与D同主族,B与C在同一周期,A,D原子的最外层电子数都是1,C原子最外层电子数比B原子少2个,且C最外层电子数是次外层电子数的2倍.A,B单质在常温下均为气体,它们在高温下以体积比2:1完全反应,生成物在常温下是液体.此液体与D单质能剧烈反应生成A的单质.所得溶液滴入酚酞显红色,同时溶液中含有与氖原子的电子层结构相同的阳离子.回答下列问题:
(1)写出B元素位于周期表中的位置 .
(2)写出CB2与D2B2反应的化学方程式 .
(3)用电子式表示化合物 A2B2 的形成过程:
(4)由A,B,C,D组成的一种化合物既可与盐酸反应又可与氢氧化钠反应,请写出其与氢氧化钠溶液反应的离子方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 熵增大的反应一定可自发进行 B. 熵减小的反应一定可自发进行
C. ΔH<0的反应可能自发进行 D. ΔH>0的反应不可能自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组在实验室中模拟上述过程。其设计的模拟装置如下:

根据要求填空:
(1)B装置有三种功能:①均匀混合气体;② ;③ 。
(2)设V(Cl2)/V(CH4)=x,若理论上欲获得最多的氯化氢,则x值应 。
(3)D装置的石棉中均匀混有KI粉末,其作用是 。
(4)E装置的作用是 (填编号)。
A.收集气体 B.吸收氯气
C.防止倒吸 D.吸收氯化氢
(5)E装置除生成盐酸外,还含有有机物,从E中分离出盐酸的最佳方法为 (填分离方法名称)。
(6)该装置还有缺陷,原因是没有进行尾气处理,其尾气主要成分为 (填编号)。
A.CH4B.CH3C1 C.CH2C12D.CHCl3E.CCl4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是25℃时某些盐的溶度积常数和弱酸的电离平衡常数,下列说法正确的是( )
化学式 | CH3COOH | H2CO3 | AgCl | Ag2CrO4 |
Ka或Ksp | Ka=1.8×10-5 | Ka1=4.1×10-7 Ka2=5.6×10-11 | Ksp=1.8×10-10 | Ksp=2.0×10-12 |
A. 常温下,相同浓度①CH3COONH4 ②NH4HCO3 ③(NH4)2CO3溶液中,c(NH4+)由大到小的顺序是:①>②>③
B. AgCl 易溶于氨水难溶于水,所以AgCl 在氨水中的Ksp 大于水中的 Ksp
C. 向饱和氯水中滴加NaOH 溶液至溶液刚好为中性时,c(Na+)=2c(ClO-)+c(HClO)
D. 向浓度均为1×10-3molL-1的KCl 和K2CrO4混合液中滴加1×10-3molL-1 的AgNO3溶液,CrO42-先形成沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com