
可以用如右图所示装置干燥、收集及尾气处理的气体是
①H2S ②HCl ③NH3 ④Cl2 ⑤SO2 ⑥C2H4
A.①和② B.②和⑤ C.③和④ D.⑤和⑥

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
以苯酚为原料的合成路线如下所示,部分试剂和反应条件已略去。请按要求作答:

(1)写出以下物质的结构简式:
B: ; F: ;
(2)写出反应④⑤的化学反应方程式:
④
⑤
(3)在苯酚钠溶液中通入少量二氧化碳气体会出现浑浊,反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(一)根据要求回答下列问题:
①CaBr2 ②H2O ③NH4Cl ④H2O2 ⑤Na2O2 ⑥Ca(OH)2 ⑦HClO ⑧I2 ⑨He
(1)含有共价键的离子化合物是(用序号回答)__________含有共价键的共价化合物是(用序号回答)________________
(2) 当其熔化时,不破坏化学键的是(用序号回答)________________
(二)写出下列物质或微粒的电子式:
H2O Na2O CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于σ键和π键的理解不正确的是( )
A.气体单质中一定存在σ键,可能存在π键
B.σ键可以绕键轴旋转,π键一定不能绕键轴旋转
C.双键中一定有一个σ键,一个π键,三键中一定有一个σ键,两个π键
D.σ键能单独存在,而π键一定不能单独存在
查看答案和解析>>
科目:高中化学 来源: 题型:
二甲醚是一种重要的清洁燃料,可替代氟利昂作制冷剂,对臭氧层无破坏作用。工业上可利用水煤气合成二甲醚,总反应为:
3H2(g)+3CO(g) CH3OCH3(g)+CO2(g) ΔH=-246.4 kJ/mol
CH3OCH3(g)+CO2(g) ΔH=-246.4 kJ/mol
(1)在一定条件下的密闭容器中,该总反应达到平衡,只改变一个条件能同时提高反应速率和CO的转化率的是________(填字母代号)。
a.降低温度 b.加入催化剂 c.缩小容器体积 d.增加H2的浓度 e.增加CO的浓度
(2)该反应的化学平衡常数表达式K= 。
温度升高平衡常数 (填“变大”、“变小”、“不变”)
(3)在一体积可变的密闭容器中充入3 mol H2、3 mol CO、1 mol CH3OCH3、1 mol CO2,在一定温度和压强下发生反应:3H2(g)+3CO(g)  CH3OCH3(g)+CO2(g),经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。
CH3OCH3(g)+CO2(g),经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。
问:①反应开始时正、逆反应速率的大小:v(正)________v(逆)(填“>”“<”或“=”),理由是
。
②平衡时n(CH3OCH3)=________,平衡时CO的转化率为________。
③在该反应条件下能判断反应达到化学平衡状态的依据是________(填编号)。
A.v(CO)=3v(CO2) B.生成a mol CO2的同时消耗3a mol H2
C.c(CO2)=c(CO) D.混合气体的平均相对分子质量不变
E.气体的密度不再改变 F.气体的总质量不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
2013年全国各地都遭遇“十面霾伏”。其中,机动车尾气和燃煤产生的烟气对空气质量恶化贡献较大。
⑴汽车尾气净化的主要原理为:2NO(g) + 2CO(g) 2CO2(g)+ N2(g)。△H<0
2CO2(g)+ N2(g)。△H<0
若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是 (填代号)。
(下图中υ正、K、n、w分别表示正反应速率、平衡常数、物质的量、质量分数)

(2)机动车尾气和煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOX可以消除氮氧化物的污染。已知:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ/mol
2NO2(g) N2O4(g) △H=-56.9 kJ/mol
N2O4(g) △H=-56.9 kJ/mol
H2O(g) = H2O(l) ΔH = -44.0 kJ/mol
 写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式: 。
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式: 。
(3)用NH3催化还原NOX也可以消除氮氧化物的污染。右图,采用NH3作还原剂,烟气以一定的流速通过两种不同催化剂,测量逸出气体中氮氧化物含量,从而确定烟气脱氮率(注:脱氮率即氮氧化物转化率),
反应原理为:
NO(g) +NO2(g)+2NH3(g) 2N2(g) + 3H2O(g)。
2N2(g) + 3H2O(g)。
①该反应的△S 0,△H 0(填“>”、“=”或 “<”)。
②对于气体反应,用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)也可以表示平衡常数(记作KP),
则上述反应的KP= 。
③以下说法正确的是 。
 A.第②种催化剂比第①种催化剂脱氮率高
A.第②种催化剂比第①种催化剂脱氮率高
B.相同条件下,改变压强对脱氮率没有影响
C.催化剂①、②分别适合于250℃和450℃左右脱氮
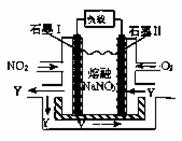
(4)NO2、O2和熔融NaNO3可制作燃料电池,其原理见右图。该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应为 。
(5)硝酸工业尾气中氮氧化物(NO和NO2)可用尿素〔CO(NH2)2〕溶液除去。反应生成对大气无污染的气体。1 mol尿素能吸收工业尾气中氮氧化物(假设NO、NO2体积比为1:1)的质量为___________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是
A.氮的氧化物是汽车尾气中的主要污染物之一
B.氮的氧化物既可形成酸雨,又是光化学污染的主要成分
C.化石燃料的燃烧是造成空气中二氧化硫含量增多的主要因素
D.酸雨在空气中静置一段时间后,雨水的酸性会慢慢减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙、丙、丁四种物质(可以是溶液)中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系: 。按要求回答下列问题:
。按要求回答下列问题:
(1)若甲为碳,则乙为________(填化学式,下同),丙为_________。
(2)若甲为氯气,则丁为_______,丙为_________。
(3)若甲为二氧化硫,丁为氢氧化钠溶液,则丙→乙的离子方程式为_____________。
(4)若甲为氯化铝溶液,丁为氢氧化钠溶液,则乙→丙的离子方程式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在MgCl2、KCl、K2SO4三种盐的混合溶液中,若K+、Cl-各为1.5mol,Mg2+为0.5mol,则SO42-的物质的量为………………………………………………………………( )
A.0.1mol B.0.5mol C.0.15mol D.0.25mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com