
(10分)金属铬和氢气在工业上都有重要的用途。已知:铬能与稀硫酸反应,生成氢气和硫酸亚铬(CrSO4)。

(1)铜铬构成原电池如右图1,其中盛稀硫酸烧杯中的现象为: 。盐桥中装的是饱和KCl琼脂溶液,下列关于此电池的说法正确的是:
A.盐桥的作用是使整个装置构成通路、保持溶液呈电中性,凡是有盐桥的原电池,盐桥中均可以用饱和KCl琼脂溶液
B.理论上1molCr溶解,盐桥中将有2molCl-进入左池,2molK+进入右池
C.此过程中H+得电子,发生氧化反应
D.电子从铬极通过导线到铜极,又通过盐桥到转移到左烧杯中
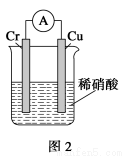
(2)如构成图2电池发现,铜电极上不再有图1的现象,铬电极上产生大量气泡,遇空气呈红棕色。写出正极电极反应式: 。
(3)某同学把已去掉氧化膜的铬片直接投入氯化铜溶液时,观察到了预料之外的现象:①铬片表面上的铜没有紧密吸附在铬片的表面而是呈蓬松的海绵状;②反应一段时间后有大量气泡逸出,且在一段时间内气泡越来越快,经点燃能发出爆鸣声,证明是氢气。请解释这两种现象的原因___________。
(1)铜电极上有气泡产生;(2分) B(2分) (2)4H++NO3-+3e-=NO↑+2H2O(2分)
(3)Cu2+的水解使溶液呈酸性,铬与酸性溶液反应生成氢气,气泡使生成的铜疏松;(2分)生成的铜和铬形成原电池,使产生氢气的速率加快。(2分)
【解析】
试题分析:(1)铜铬构成原电池如右图1,由于铬能与稀硫酸反应,生成氢气和硫酸亚铬(CrSO4),这说明铬电极是负极,铜电极是正极,氢离子放电,所以盛稀硫酸烧杯中的现象为铜电极上有气泡产生;A.盐桥的作用是使整个装置构成通路、保持溶液呈电中性,当盐桥中不一定均可以用饱和KCl琼脂溶液,A错误;B.理论上1molCr溶解,则转移2mol电子生成1molCr2+,同时消耗2mol氢离子,所以根据溶液的电中性可知盐桥中将有2molCl-进入左池,2molK+进入右池,B正确;C.此过程中H+得电子,发生还原反应,C错误;D.电子不能在溶液中传递,D错误,答案选B。
(2)如构成图2电池发现,铜电极上不再有图1的现象,铬电极上产生大量气泡,遇空气呈红棕色,说明溶液中的硝酸根得到电子,产生NO,NO被氧化生成NO2,因此铜是负极,铬是正极,则正极电极反应式4H++NO3-+3e-=NO↑+2H2O。
(3)由于Cu2+的水解使溶液呈酸性,铬与酸性溶液反应生成氢气,气泡使生成的铜疏松。生成的铜和铬形成原电池,因此使产生氢气的速率加快。
考点:考查电化学原理的应用


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015吉林省高一上学期期末考试化学试卷(解析版) 题型:填空题
(10分)非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,请回答下列问题:

(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
①D物质的名称是________;请写出由B转化成 C的化学方程式____________________________
②在工业生产中大量排放的B气体被雨水吸收后形成了________而污染了环境。
(2)若A在常温下为气体,C是红棕色的气体。
①A、C的化学式分别是:A________;C________.请写出由C与H2O生成 D的化学方程式
____________________________________________________
②D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的离子方程式___________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015吉林省高一上学期期末考试化学试卷(解析版) 题型:选择题
不能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是
A.分别加热这两种固体物质,并将生成的气体通人澄清的石灰水中
B.分别在这两种固体中,加入同浓度的稀盐酸
C.分别在这两种物质的溶液中,加入CaCl2溶液
D.分别在这两种物质的溶液中,加入少量澄清的石灰水
查看答案和解析>>
科目:高中化学 来源:2014-2015吉林省高一上学期期末考试化学试卷(解析版) 题型:选择题
下列说法正确的是
①氯气的性质活泼,它与氢气混合后立即发生爆炸
②实验室制取氯气时,为了防止环境污染,多余的氯气可以用氢氧化钙溶液吸收
③新制氯水的氧化性强于久置氯水
④除去Cl2气体中的HCl,可将气体通入饱和食盐水
⑤检验HCl气体中是否混有Cl2的方法是将气体通入硝酸银溶液
A.①②③ B.②③④ C.③④ D.③
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三第一次五校联考化学试卷(解析版) 题型:选择题
在甲、乙、丙三个不同密闭容器中按不同方式投料,一定条件下发生反应(起始温度和起始体积相同):N2(g)+3H2(g) 2NH3(g) ΔH<0,相关数据如下表所示:
2NH3(g) ΔH<0,相关数据如下表所示:
容器 | 甲 | 乙 | 丙 |
相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
反应物投料 | 1mol N2、3mol H2 | 2mol NH3 | 2mol NH3 |
平衡时容器体积 | V甲 | V乙 | V丙 |
反应的平衡常数K= | K甲 | K乙 | K丙 |
平衡时NH3的浓度/mol·L-1 | c甲 | c乙 | c丙 |
平衡时NH3的反应速率/mol·L-1·min-1 | v甲 | v乙 | v丙 |
下列说法正确的是
A.V甲>V丙 B.K乙<K丙 C.c乙>c甲 D.v甲=v丙
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三第一次五校联考化学试卷(解析版) 题型:选择题
现有室温下的四种溶液,其pH如下表所示,下列有关叙述不正确的是
① | ② | ③ | ④ | |
pH | 11 | 11 | 3 | 3 |
溶液 | 氨水 | NaOH溶液 | 醋酸 | 盐酸 |
A.③④中分别加入适量醋酸钠晶体,两溶液pH均增大
B.②③两溶液等体积混合,所得溶液中:c(H+)>c(OH-)
C.分别加水稀释10倍,溶液的pH:①>②>④>③
D.V1L④和V2L①溶液混合后,若pH=7,则V1<V2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省潍坊市高三12月月考化学试卷(解析版) 题型:选择题
在标准状况下,将a L NH3完全溶于水得到V mL氨水,溶液的密度为ρg·cm-3,溶质的质量分数为w,溶质的物质的量浓度为c mol·L-1。下列叙述中正确的是
①
②
③若上述溶液中再加入V mL水后,所得溶液的质量分数大于0.5w
④将50g上述溶液加入一定量的水稀释成0.5 c mol·L-1,则加入水的体积应大于50mL
A.①④ B.②③ C.①③ D.②④
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省新余市高三上学期期末考试理综化学试卷(解析版) 题型:选择题
常温下,下列溶液的pH或微粒的物质的量浓度关系正确的是
A.某溶液中由水电离出的c(OH-) = 1×10-amol·L-1,若a>7时,则该溶液的pH一定为14-a
B.等体积、等物质的量浓度的Na2SO3溶液与NaHSO3溶液混合:c(Na+) = c(SO32-) + c(HSO3-) + c(H2SO3)
C.将0.2mol·L-1的某一元酸HA溶液和0.1mol·L-1的NaOH溶液等体积混合后溶液的pH大于7,则反应后的混合液:2c(OH-)+c(A-)=2c(H+)+c(HA)
D.pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后,混合液的pH等于7,则反应后的混合液:c(Na+)>2c(R2-)+c(HR-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com