
ΓΨΧβΡΩΓΩAΓΔBΓΔCΓΔD «ΥΡ÷÷≥ΘΦϊΒΡ”–ΜζΈοΘ§Τδ÷–A «“Μ÷÷ΤχΧ§ΧΰΘ§‘Ύ±ξΉΦΉ¥Ωωœ¬ΒΡΟήΕ»ΈΣ1.25g/LΘΜB”κC‘Ύ≈®ΝρΥαΚΆΦ”»»ΧθΦΰœ¬ΖΔ…ζΖ¥”ΠΘ§…ζ≥…ΒΡ”–ΜζΈο”–ΧΊ βœψΈΕΘΜAΓΔBΓΔCΓΔD‘Ύ“ΜΕ®ΧθΦΰœ¬ΒΡΉΣΜ·ΙΊœΒ»γΆΦΥυ ΨvΘ®Ζ¥”ΠΧθΦΰ“― Γ¬‘Θ©ΘΚ 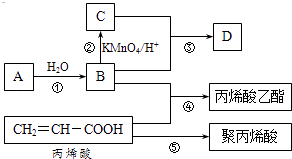
Θ®1Θ©AΒΡΒγΉ” ΫΈΣ Θ§ C÷–ΙΌΡήΆ≈ΒΡΟϊ≥ΤΈΣ Θ°
Θ®2Θ©±ϊœ©ΥαΘ®CH2=CH©¹COOHΘ©ΒΡ–‘÷ Ω…Ρή”– Θ°
aΘ°Φ”≥…Ζ¥”Π bΘ°»Γ¥ζΖ¥”Π cΘ°Φ”ΨέΖ¥”Π dΘ°÷–ΚΆΖ¥”Π eΘ°―θΜ·Ζ¥”Π
Θ®3Θ©”ΟΝΫ÷÷ΖΫΖ®Φχ±πBΚΆCΘ§Υυ”Ο ‘ΦΝΖ÷±π «ΓΔ Θ°
Θ®4Θ©±ϊœ©Υα““θΞΒΡΫαΙΙΦρ ΫΈΣ Θ°
Θ®5Θ©–¥≥ωœ¬Ν–Ζ¥”ΠΖΫ≥Χ ΫΚΆ”–ΜζΖ¥”ΠΜυ±Ψάύ–ΆΘΚ
ΔΌ Θ§ Ζ¥”ΠΘΜ
Δή Θ§ Ζ¥”ΠΘΜ
Δί Θ§ Ζ¥”ΠΘ°
ΓΨ¥πΑΗΓΩ
Θ®1Θ©![]() ΘΜτ»Μυ
ΘΜτ»Μυ
Θ®2Θ©abcde
Θ®3Θ©Υα–‘ΗΏΟΧΥαΦΊ»ή“ΚΘΜΧΦΥα«βΡΤ»ή“Κ
Θ®4Θ©CH2=CH©¹COOCH2CH3
Θ®5Θ©CH2=CH2+H2O ![]() CH3CH2OHΘΜΦ”≥…ΘΜCH2=CHCOOH+HOCH2CH3
CH3CH2OHΘΜΦ”≥…ΘΜCH2=CHCOOH+HOCH2CH3 ![]() CH2=CHCOOCH2CH3+H2OΘΜθΞΜ·Μρ»Γ¥ζΘΜnCH2=CH©¹COOH
CH2=CHCOOCH2CH3+H2OΘΜθΞΜ·Μρ»Γ¥ζΘΜnCH2=CH©¹COOH ![]()
 ΘΜΦ”Ψέ
ΘΜΦ”Ψέ
ΓΨΫβΈωΓΩΫβΘΚAΓΔBΓΔCΓΔD «ΥΡ÷÷≥ΘΦϊΒΡ”–ΜζΈοΘ§Τδ÷–A «“Μ÷÷ΤχΧ§ΧΰΘ§‘Ύ±ξΉΦΉ¥Ωωœ¬ΒΡΟήΕ»ΈΣ1.25g/LΘ§ΤδΡΠΕϊ÷ ΝΩ=1.25g/LΓΝ22.4L/mol=28g/molΘ§BΚΆ±ϊœ©ΥαΖΔ…ζθΞΜ·Ζ¥”Π…ζ≥…±ϊœ©Υα““θΞΘ§‘ρBΈΣCH3CH2OHΘ§B±ΜΥα–‘ΗΏΟΧΥαΦΊ»ή“Κ―θΜ·…ζ≥…CΈΣCH3COOHΘ§B”κC‘Ύ≈®ΝρΥαΚΆΦ”»»ΧθΦΰœ¬ΖΔ…ζΖ¥”ΠΘ§…ζ≥…ΒΡ”–ΜζΈο”–ΧΊ βœψΈΕΘ§‘ρDΈΣCH3COOCH2CH3ΘΜ““œ©ΚΆΥ°ΖΔ…ζΦ”≥…Ζ¥”Π…ζ≥…““¥ΦΘ§‘ρAΈΣCH2=CH2ΘΜ±ϊœ©ΥαΖΔ…ζΦ”ΨέΖ¥”Π…ζ≥…Ψέ±ϊœ©Υα.
Θ®1.Θ©A «““œ©Θ§““œ©Ζ÷Ή”ΒγΉ” ΫΈΣ ![]() Θ§C «““ΥαΘ§““Υα÷–ΙΌΡήΆ≈Οϊ≥Τ «τ»ΜυΘ§Υυ“‘¥πΑΗ «ΘΚ
Θ§C «““ΥαΘ§““Υα÷–ΙΌΡήΆ≈Οϊ≥Τ «τ»ΜυΘ§Υυ“‘¥πΑΗ «ΘΚ ![]() ΘΜτ»ΜυΘΜ
ΘΜτ»ΜυΘΜ
Θ®2.Θ©aΘ°±ϊœ©Υα÷–ΧΦΧΦΥΪΦϋΡήΦ”≥…Ζ¥”ΠΘ§Ι ’ΐ»ΖΘΜ
bΘ°±ϊœ©Υα÷–τ»ΜυΡήΖΔ…ζ»Γ¥ζΖ¥”ΠΘ§Ι ’ΐ»ΖΘΜ
cΘ°±ϊœ©Υα÷–ΧΦΧΦΥΪΦϋΡήΖΔ…ζΦ”ΨέΖ¥”ΠΘ§Ι ’ΐ»ΖΘΜ
dΘ°±ϊœ©Υα÷–τ»ΜυΡήΖΔ…ζ÷–ΚΆΖ¥”ΠΘ§Ι ’ΐ»ΖΘΜ
eΘ°±ϊœ©Υα÷–ΧΦΧΦΥΪΦϋΡήΖΔ…ζ―θΜ·Ζ¥”ΠΘ§Ι ’ΐ»ΖΘΜΙ ―Γa b c d eΘΜ
Θ®3.Θ©B «““¥ΦΓΔC «““ΥαΘ§““¥ΦΡή±ΜΥα–‘ΗΏΟΧΥαΦΊ»ή“Κ―θΜ·Εχ ΙΥα–‘ΗΏΟΧΥαΦΊ»ή“ΚΆ …ΪΘ§ΒΪ““Υα≤ΜΡή ΙΥα–‘ΗΏΟΧΥαΦΊ»ή“ΚΆ …ΪΘ§““ΥαΡήΚΆΧΦΥα«βΡΤΖ¥”Π…ζ≥…Εΰ―θΜ·ΧΦΘ§ΒΪ““¥Φ≤ΜΡήΘ§Υυ“‘Ω…“‘”ΟΧΦΥα«βΡΤ»ή“ΚΓΔΥα–‘ΗΏΟΧΥαΦΊ»ή“ΚΦχ±πΕΰ’ΏΘ§Υυ“‘¥πΑΗ «ΘΚNaHCO3»ή“ΚΘΜKMnO4Υα–‘»ή“ΚΘΜ
Θ®4.Θ©±ϊœ©ΥαΚΆ““¥ΦΖ¥”Π…ζ≥…±ϊœ©Υα““θΞΘ§ΤδΫαΙΙΦρ ΫΈΣCH2=CH©¹COOCH2CH3 Θ§ Υυ“‘¥πΑΗ «ΘΚCH2=CH©¹COOCH2CH3ΘΜ
Θ®5.Θ©ΔΌΈΣ““œ©ΚΆΥ°ΒΡΦ”≥…Ζ¥”ΠΘ§Ζ¥”ΠΖΫ≥Χ ΫΈΣCH2=CH2+H2O ![]() CH3CH2OHΘ§ΈΣΦ”≥…Ζ¥”ΠΘΜΔήΈΣ±ϊœ©ΥαΚΆ““¥ΦΒΡθΞΜ·Ζ¥”ΠΘ§Ζ¥”ΠΖΫ≥Χ ΫΈΣCH2=CHCOOH+HOCH2CH3
CH3CH2OHΘ§ΈΣΦ”≥…Ζ¥”ΠΘΜΔήΈΣ±ϊœ©ΥαΚΆ““¥ΦΒΡθΞΜ·Ζ¥”ΠΘ§Ζ¥”ΠΖΫ≥Χ ΫΈΣCH2=CHCOOH+HOCH2CH3 ![]() CH2=CHCOOCH2CH3+H2OΘ§ΈΣθΞΜ·Ζ¥”ΠΜρ»Γ¥ζΖ¥”ΠΘ§ΔίΈΣ±ϊœ©ΥαΖΔ…ζΒΡΦ”ΨέΖ¥”ΠΘ§Ζ¥”ΠΖΫ≥Χ ΫΈΣn CH2=CH©¹COOH
CH2=CHCOOCH2CH3+H2OΘ§ΈΣθΞΜ·Ζ¥”ΠΜρ»Γ¥ζΖ¥”ΠΘ§ΔίΈΣ±ϊœ©ΥαΖΔ…ζΒΡΦ”ΨέΖ¥”ΠΘ§Ζ¥”ΠΖΫ≥Χ ΫΈΣn CH2=CH©¹COOH ![]()
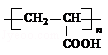 Θ§ΈΣΦ”ΨέΖ¥”ΠΘ§Υυ“‘¥πΑΗ «ΘΚΔΌCH2=CH2+H2O
Θ§ΈΣΦ”ΨέΖ¥”ΠΘ§Υυ“‘¥πΑΗ «ΘΚΔΌCH2=CH2+H2O ![]() CH3CH2OHΘΜ Φ”≥…ΘΜΔήCH2=CHCOOH+HOCH2CH3
CH3CH2OHΘΜ Φ”≥…ΘΜΔήCH2=CHCOOH+HOCH2CH3 ![]() CH2=CHCOOCH2CH3+H2OΘΜθΞΜ·/»Γ¥ζΔίn CH2=CH©¹COOH
CH2=CHCOOCH2CH3+H2OΘΜθΞΜ·/»Γ¥ζΔίn CH2=CH©¹COOH ![]()
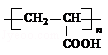 ΘΜΦ”ΨέΘ°
ΘΜΦ”ΨέΘ°


 ΧλΧλœρ…œ“Μ±ΨΚΟΨμœΒΝ–¥πΑΗ
ΧλΧλœρ…œ“Μ±ΨΚΟΨμœΒΝ–¥πΑΗ –Γ―ß…ζ10Ζ÷÷””Π”ΟΧβœΒΝ–¥πΑΗ
–Γ―ß…ζ10Ζ÷÷””Π”ΟΧβœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΧζΓΔΆ≠ΦΑΤδΜ·ΚœΈο‘Ύ»’≥Θ…ζ≤ζΓΔ…ζΜν÷–”–Ή≈ΙψΖΚΒΡ”Π”ΟΓΘΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©Χζ‘ΣΥΊ‘Ύ÷ήΤΎ±μ÷–ΒΡΈΜ÷Ο «_______Θ§ΜυΧ§Cu2+ΒΡΚΥΆβΒγΉ”≈≈≤Φ Ϋ «__________ΓΘ‘ΣΥΊΧζ”κΆ≠ΒΡΒΎΕΰΒγάκΡήΖ÷±πΈΣΘΚICu=1958 kJΓΛmol-1ΓΔIFe=1561 kJΓΛmol-1Θ§ICuΘΨIFeΒΡ‘≠“ρ «_________________ΓΘ
Θ®2Θ©”–ΜζΧζΖ »ΐœθΥαΝυΡρΥΊΚœΧζ(Δσ)Θ§Μ·―ß ΫΈΣΘΚ[Fe(H2NCONH2)6](NO3)3ΓΘ
ΔΌΡρΥΊΖ÷Ή”÷–C‘≠Ή”ΒΡ‘”Μ·ΖΫ Ϋ «__________ΓΘ
ΔΎ[Fe(H2NCONH2)6](NO3)3 ÷–ΓΑH2NCONH2Γ±”κ Fe(Δσ)÷°ΦδΒΡΉς”ΟΝΠ «_______ΓΘΗυΨίΦέ≤ψΒγΉ”Ε‘ΜΞ≥βάμ¬έΆΤ≤β NO3Θ≠ΒΡΩ’ΦδΙΙ–ΆΈΣ____________ΓΘ
Θ®3Θ©Fe3+Ω…”ΟSCNΘ≠Φλ―ιΘ§ΤδΕ‘”ΠΒΡΥα”–ΝΫ÷÷Θ§Ζ÷±πΈΣΝρ«ηΥαΘ®H-S-CΓ‘NΘ©ΚΆ“λΝρ«ηΥαΘ®H-N=C=SΘ©Θ§’βΝΫ÷÷Υα÷–Ζ–ΒψΫœΗΏΒΡ «_______Θ§ ‘≠“ρ «______________ΓΘ
Θ®4Θ©FeCl3ΨßΧε“Ή»ή”ΎΥ°ΚΆ““¥ΦΘ§”ΟΨΤΨΪΒΤΦ”»»Φ¥Ω…ΤχΜ·Θ§”…¥ΥΩ…÷Σ FeCl3ΒΡΨßΧεάύ–ΆΈΣ______ΘΜSΚΆFe–Έ≥…ΒΡΡ≥Μ·ΚœΈοΘ§ΤδΨßΑϊ»γΆΦ“ΜΥυ ΨΘ§ ‘ρΗΟΈο÷ ΒΡΜ·―ß ΫΈΣ__________ΓΘ

Θ®5Θ©CuΨßΧεΒΡΕ―ΜΐΖΫ Ϋ»γΆΦΕΰΥυ ΨΘ§ΨßΧε÷–Cu‘≠Ή”ΒΡ≈δΈΜ ΐΈΣ_______ΘΜ…ηCu‘≠Ή”ΑκΨΕΈΣaΘ§ΨßΧεΩ’Φδάϊ”Ο¬ ΈΣ _________Θ®”ΟΚ§a ΒΡ ΫΉ”±μ¥οΘ§≤ΜΜ·ΦρΘ©ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ‘ΎΉ‘»ΜΫγ÷–Θ§Φ»”–“‘”ΈάκΧ§–Έ Ϋ¥φ‘ΎΘ§”÷”–“‘Μ·ΚœΧ§–Έ Ϋ¥φ‘ΎΒΡ‘ΣΥΊ «Θ® Θ©
A. Νρ B. Ιη C. ¬» D. ¬Ν
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΩ…ΡφΖ¥”Π‘Ύ“ΜΕ®ΧθΦΰœ¬¥οΒΫΜ·―ßΤΫΚβΉ¥Χ§ΒΡ±ξ÷Ψ «
A. Ζ¥”ΠΆΘ÷ΙΝΥ
B. ’ΐΖ¥”ΠΥΌ¬ ”κΡφΖ¥”ΠΥΌ¬ ΨυΈΣΝψ
C. Ζ¥”ΠΈοΚΆ…ζ≥…Έο≈®Ε»œύΒ»
D. ’ΐΖ¥”ΠΥΌ¬ ”κΡφΖ¥”ΠΥΌ¬ œύΒ»
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ≤ίΥαΨßΧε(H2C2O4ΓΛ2H2O)Έό…ΪΘ§»έΒψΈΣ101Γφ,“Ή»ή”ΎΥ°Θ§ ή»»Ά―Υ°ΓΔ…ΐΜΣ,170Γφ“‘…œΖ÷ΫβΓΘΡ≥―ß…ζΡβ”Οœ¬ΆΦΉΑ÷ΟΉω≤ίΥαΨßΧεΒΡΖ÷Ϋβ Β―ι≤Δ―ι÷Λ≤ΩΖ÷≤ζΈοΘ§œ¬Ν–ΥΒΖ®¥μΈσΒΡ «
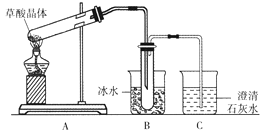
A. ΉΑ÷ΟA÷–ΒΡ¥σ ‘ΙήΩΎ”Π¬‘œρœ¬«ψ–±Θ§ «“ρΈΣΦ”»»≤ίΥαΨßΧε ±Μα≤ζ…ζΥ°
B. ΉΑ÷ΟBΒΡ÷ς“ΣΉς”Ο «άδΡΐ(Υ°’τΤχΓΔ≤ίΥα)Β»,Ζά÷Ι≤ίΥαΫχ»κΉΑ÷ΟC÷–,Η…»≈CO2ΒΡΦλ―ι
C. ΉΑ÷ΟC÷–Ω…Ιέ≤λΒΫΒΡœ÷œσ «”–Τχ≈ίΟΑ≥ω,≥Έ«ε ·Μ“Υ°±δΜκΉ«
D. ±Ψ Β―ιΡή÷ΛΟς≤ίΥαΨßΧεΒΡΖ÷Ϋβ≤ζΈο”–Εΰ―θΜ·ΧΦ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥Έ¬Ε»œ¬Θ§‘Ύ“ΜΗω2LΒΡΟή±’»ίΤς÷–Θ§Φ”»Υ4molAΚΆ2molBΫχ––»γœ¬Ζ¥”ΠΘΚ3AΘ®gΘ©+2BΘ®gΘ©![]() 4CΘ®ΘΩΘ©+2DΘ®ΘΩΘ©Θ§Ζ¥”Π“ΜΕΈ ±ΦδΚσ¥οΒΫΤΫΚβΘ§≤βΒΟ…ζ≥…1.6molCΘ§«“Ζ¥”ΠΒΡ«ΑΚσ―Ι«Ω÷°±»ΈΣ5:4Θ®œύΆ§ΒΡΈ¬Ε»œ¬≤βΝΩΘ©Θ§‘ρœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
4CΘ®ΘΩΘ©+2DΘ®ΘΩΘ©Θ§Ζ¥”Π“ΜΕΈ ±ΦδΚσ¥οΒΫΤΫΚβΘ§≤βΒΟ…ζ≥…1.6molCΘ§«“Ζ¥”ΠΒΡ«ΑΚσ―Ι«Ω÷°±»ΈΣ5:4Θ®œύΆ§ΒΡΈ¬Ε»œ¬≤βΝΩΘ©Θ§‘ρœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
AΘ°ΗΟΖ¥”ΠΒΡΜ·―ßΤΫΚβ≥Θ ΐ±μ¥ο Ϋ «K=![]()
BΘ°¥Υ ±Θ§BΒΡΤΫΚβΉΣΜ·¬ «35ΘΞ
CΘ° ‘ωΦ”CΘ§BΒΡΤΫΚβΉΣΜ·¬ ≤Μ±δ
DΘ°‘ω¥σΗΟΧεœΒΒΡ―Ι«ΩΘ§ΤΫΚβœρ”““ΤΕ·Θ§Μ·―ßΤΫΚβ≥Θ ΐ‘ω¥σ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–Υ°»ή“Κ÷–ΒΡΒγάκΖΫ≥Χ Ϋ’ΐ»ΖΒΡ «
ΔΌNaHCO3=Na++H++CO32-
ΔΎNaHSO4=Na++H++SO42-
ΔέH2SO4=2H++SO42-
ΔήKClO3=K++Cl5++3O2-
A. ΔΎΔέ B. ΔΎ C. ΔΌΔή D. Δέ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩSO2ΖœΤχΒΡΜΊ ’άϊ”ΟΖΫΑΗ»γΆΦΥυ ΨΓΘœ¬Ν–ΥΒΖ®¥μΈσΒΡ «
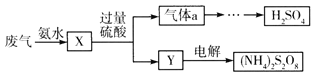
A. ΖœΤχ”κΑ±Υ°ΜλΚœ“ΜΕ®ΖΔ…ζΖ¥”ΠΘΚ2NH3ΓΛH2O+SO2===2NH4++SO32Θ≠+H2O
B. Y÷–Κ§”–NH4HSO3
C. ΤχΧεaΦ»”–―θΜ·–‘”÷”–ΜΙ‘≠–‘
D. (NH4)2S2O8÷–Κ§”–O-OΦϋ,SΒΡΜ·ΚœΦέΈΣ+6
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬ΆΦΈΣ–Υ»Λ–ΓΉι…ηΦΤΒΡ““¥Φ―θΜ·ΒΡ Β―ιΉΑ÷ΟΆΦ(Φ”»»“«ΤςΘ§Φ–≥÷ΉΑ÷Ο¬‘)ΓΘ
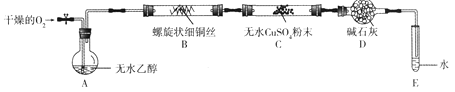
“―÷Σ:““¥ΦΒΡΖ–ΒψΈΣ78ΓφΘ§“Ή»ή”ΎΥ°Θ§““»©ΒΡΖ–ΒψΈΣ20.8Γφ,“Ή»ή”ΎΥ°ΓΘ
Θ®1Θ©‘Ύ…œ ωΉΑ÷Ο÷–, Β―ι ±Υυ–ηΦ”»»ΒΡ“«Τς÷–”ΠΉνœ»Φ”»»ΒΡ «______(Χν“«ΤςΒΡ¥ζΚ≈)ΓΘ
Θ®2Θ© ΙA÷–““¥Φ≤ζ…ζ’τΤχΒΡ≥Θ”ΟΖΫΖ® «_________________ΓΘDΉΑ÷ΟΒΡΉς”Ο «______ΓΘ
Θ®3Θ©EΉΑ÷ΟΒΡ…ηΦΤΡΩΒΡ «_________________ΓΘ
Θ®4Θ©÷ΛΟς““¥ΦΖ¥”ΠΚσ”–““»©…ζ≥…ΒΡΖΫΖ® «_________________ΓΘ
Θ®5Θ©–¥≥ωBΉΑ÷Ο÷–ΖΔ…ζΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ: _________________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com