
常温下,在下列指定条件的各溶液中,一定能大量共存的离子组是
A.中性溶液中:K+、Fe3+、ClO-、SO42-
B.pH<7的溶液中:Na+、Ba2+、Br-、Cl-
C.加入金属镁能产生H2的溶液中:Na+、Fe2+、SO42-、NO3-
D.c(H+)/c(OH-)=10-12的溶液中:K+、NH4+、HCO3-、NO3-
科目:高中化学 来源:2015-2016学年吉林省高二上学期期中(文)化学试卷(解析版) 题型:填空题
在300 ml 2 mol·L-1 H2SO4溶液中,H+的浓度是______,H+的物质的量是______,SO42-的数目是________。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省富阳市高三上学期第二次质检化学试卷(解析版) 题型:选择题
取未知浓度的硫酸、盐酸和醋酸各25.00mL,分別用0.10mol·L-1的NaOH溶液或0.10mol·L-1 的稀氨水滴定得下图。下列说法正确的是
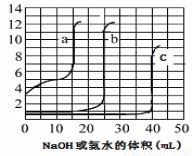
A.由图可知曲线c为NaOH滴定硫酸
B.由图可知硫酸的物质的量浓度大于盐酸的物质的量浓度
C.曲线b、c的滴定实验可用酚酞做指示剂
D.由图可知滴定前醋酸电离度约为1.67﹪
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林实验中学高一上学期期中考试化学试卷(解析版) 题型:选择题
下列说法中正确的是( )
A.纯净物一定由分子 构成
构成
B.由同种分子构成的物质一定是纯净物
C.混合物肯定是由两种以上的元素组成的
D.含有氧元素的化合物就是氧化物
查看答案和解析>>
科目:高中化学 来源:2016届浙江嘉兴第一中学高三上学期能力测试理综化学试卷(解析版) 题型:实验题
乙酰苯胺是常用的医药中间体,可由苯胺与乙酸制备。反应的化学方程式如下:

有关化合物的物理性质见下表:
化合物 | 密度(g.cm-3) | 溶解性 | 熔点(℃) | 沸点(℃) |
乙酸 | 1.05 | 易溶于水、乙醇 | 17 | 118 |
苯胺 | 1.02 | 微溶于水,易溶于乙醇 | -6 | 184 |
乙酰苯胺 | - | 微溶于冷水,可溶于热水,易溶于乙醇 | 114 | 304 |
合成:
方案甲:采用装置甲(分馏柱的作用类似于石油分馏中的分馏塔)。在圆底烧瓶中加入5.0 mL 苯胺、7.4 mL乙酸,加热至沸,控制温度计读数100 ~ 105℃, 保持液体平缓流出,反应40 min后停止加热。将圆底烧瓶中的液体趁热倒入盛有100 mL水的烧杯,冷却后有乙酰苯胺固体析出,过滤得粗产物。
方案乙:采用装置乙,加热回流,反应40 min后停止加热。其余与方案甲相同。
提纯:
甲乙两方案均采用重结晶方法。操作如下:
①加热溶解→②活性炭脱色→③趁热过滤→④冷却结晶→⑤过滤→⑥洗涤→⑦干燥

装置甲 装置乙
请回答:
(1)仪器a的名称是 ,b处水流方向是 (填“进水”或“出水”)。
(2)合成步骤中,乙酰苯胺固体析出后,过滤分离出粗产物。留在滤液中的主要物质是 。
(3)提纯过程中的第③步,过滤要趁热的理由是 。
(4)提纯过程第⑥步洗涤,下列洗涤剂中最合适的是 。
A.蒸馏水 B.乙醇 C.5%Na2CO3溶液 D.饱和NaCl溶液
(5)从投料量分析,为提高乙酰苯胺产率,甲乙两种方案均采取的措施是 ;实验结果表明方案甲的产率较高,原因是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高二上学期期中测试化学试卷(解析版) 题型:填空题
Ⅰ.用稀盐酸与稀NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
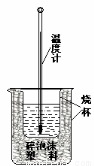
(1)该图中有两处未画出,它们是烧杯上方的泡沫塑料盖和_ 。泡沫塑料的作用是 。
(2)若稀盐酸用相同体积的下列溶液代替,则对中和热数值测定结果将如何影响(填“偏大”、“偏小”、“无影响”):浓硫酸 ;稀硝酸 ;醋酸溶液 。
Ⅱ.如图所示,把试管放入盛有25℃饱和石灰水的烧杯中,试管开始放入几小块镁片,再用滴管滴入5mL盐酸于试管
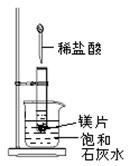
(1)写出有关的离子方程式:______________________ 。
(2)烧杯中出现的现象为: 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高二上学期期中测试化学试卷(解析版) 题型:实验题
)某课外活动小组同学用右图装置进行实验,试回答下列问题。
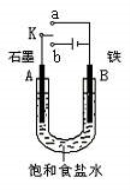
(1)若开始时开关K与a连接,则A极的电极反应式为:________________________。
(2)若开始时开关K与b连接,则B极的电极反应式为:_________________________, 总反应的离子方程式为___________________。 有关上述实验,下列说法正确的是(填序号)______________
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润KI淀粉试纸变蓝
③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度(饱和食盐水足量)
④若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(3)该小组同学模拟工业上用离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阳极反应式为_____________。此时通过阴离子交换膜的离子数____________(填“大于”或“小于”或“等于”)通过阳离子交换膜的离子数。
②制得的硫酸溶液从出口(填写“A”、“B”、“C”、“D”)_____________导出。
③通电开始后,阴极附近溶液pH会增大,请简述原因__________________ 。
④若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的电极反应式为___________________。
查看答案和解析>>
科目:高中化学 来源:2016届江苏省淮安市高三上学期10月阶段测化学试卷(解析版) 题型:选择题
某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制取七水合硫酸亚铁(FeSO4·7H2O),设计了如下流程:
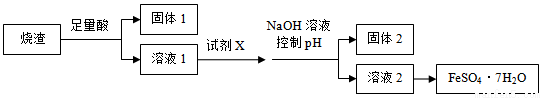
下列说法不正确的是
A、溶解烧渣选用足量硫酸,试剂X选用铁粉
B.固体1中一定含有SiO2,控制pH是为了使Al3+转化为A1(OH)3,进入固体2
C、从溶液2得到FeSO4·7H2O产品的过程中,须控制条件防止其氧化和分解
D、若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO4·7H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com