
不能作为判断硫、氯两种元素非金属性强弱的依据是
A.单质氧化性的强弱 B.氢化物沸点的高低
C.氢化物还原性强弱 D.最高价氧化物对应的水化物酸性的强弱
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源:2015-2016学年湖北省高二第一学期第一次月考化学试卷(解析版) 题型:填空题
(10分) (1)远洋轮船的钢铁船体在海水中易发生电化学腐蚀中的________腐蚀。为防止这种腐蚀,通常把船体与浸在海水里的Zn块相连,或与像铅酸蓄电池这样的直流电源的________极(填“正”或“负”)相连。
(2)基态Fe原子有 个未成对电子,Fe2+的电子排布式为 。可用铁氰化钾溶液检验 Fe2+,发生反应的离子方程式为 。
(3)用惰性电极电解200 mL一定浓度的硫酸铜溶液(不考虑电解过程中溶液体积变化),通电一段时间后,若向所得的溶液中加入0.1 mol Cu (OH)2,溶液恰好恢复到电解前的浓度和pH,则电解过程中转移电子的物质的量为________ mol。
(4)用铂作电极电解AlCl3溶液的总反应离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期二调化学试卷(解析版) 题型:选择题
下列说法中不正确的是
A.在燃煤中加入石灰石可减少SO2排放,发生的反应为2CaCO3 +2SO2 +O2 2CO2 +2CaSO4
2CO2 +2CaSO4
B.C02通入水玻璃可以得到硅酸沉淀
C.硅主要以单质、氧化物、硅酸盐的形式存在于自然界中
D.氢氟酸能够雕刻玻璃,故不能用玻璃瓶来盛装氢氟酸
查看答案和解析>>
科目:高中化学 来源:2016届河南省高三第四次大考化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.1.0 mol·L-1的KNO3溶液:H+、Fe2+、Cl-、SO42-
B.通入过量SO2气体后的溶液:H+、Ca2+、Fe3+、NO3-
C.通入足量CO2的溶液:H+、NH4+、Al3+、SO42-
D.与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3-
查看答案和解析>>
科目:高中化学 来源:2016届河北省衡水市高三复习班上月考化学试卷(解析版) 题型:选择题
某同学做了如下两个实验:
①将少量氯气通入FeI2与淀粉的混合溶液中,溶液变蓝色;
②将少量氯气通入到FeBr2与KSCN的混合溶液中溶液变红色。
由上述实验可以得出的结论是
A.氧化性:Cl2>Fe3+>Br2>I2
B.②发生反应Fe2++Cl2=Fe3++2Cl-
C.实验中只有氯气发生氧化反应
D.实验②发生的反应中,有一个是非氧化还原反应
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三9月月考化学试卷(解析版) 题型:选择题
下列物质的检验,其结论一定正确的是
A.向某溶液中加入BaCl2溶液,产生白色沉淀,加入HNO3后,白色沉淀不溶解,也无其他现象,说明原溶液中一定含有SO42—
B.向某溶液中加盐酸产生无色气体,该气体能使澄清的 石灰水变浑浊,说明该溶液中一定含有CO32— 或SO32—
石灰水变浑浊,说明该溶液中一定含有CO32— 或SO32—
C.取少量久置的Na2SO3样品于试管中加水溶解,再加盐酸酸化,然后加BaCl2溶液,若加HCl时有气体产生,加BaCl2时有白色沉淀产生,说明Na2SO3样品已部分被氧化
D.将某气体通入品红溶液中,品红溶液退色,该气体一定是SO2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年海南华侨中学高三第一次模拟考试化学试卷(解析版) 题型:选择题
N2O5是一种新型硝化剂,在一定温度下可发生下列反应:2N2O5(g) 4NO2(g)+ O2(g) △H >0
4NO2(g)+ O2(g) △H >0
T1温度下的部分实验数据为
t/s | 0 | 500 | 1000 | 1500 |
C(N2O5)mol/L | 5.00 | 3.52 | 2.50 | 2.50 |
下列说法不正确的是
A.500s内N2O5分解速率为2.96×10-3 mol/(L·s)
B.T1温度下的平衡常数为K1=125,1000s时转化率为50%
C.T1温度下的平衡常数为K1 ,T2温度下的平衡常数为K2,若K1<K2,则T1 >T2
D.平衡后其他条件不变,将容器的体积压缩到原来的1/2,则再平衡时C(N2O5) >5.00mol/L
查看答案和解析>>
科目:高中化学 来源:2016届河南省高三上学期开学考试化学试卷(解析版) 题型:实验题
(11分)(NH4)2SO4是常用的化肥和化工原料,受热易分解。某兴趣小组拟探究其分解产物。
【查阅资料】(NH4)2SO4在260℃和400℃时分解产物不同。
【实验探究】该小组拟选用如图所示装置进行实验(夹持和加热装置略)
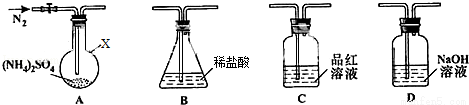
实验1:连接装置A﹣B﹣C﹣D,检查气密性,按图示加入试剂(装置B盛0.5000mol/L盐酸 70.00mL)通入N2排尽空气后,于260℃加热装置A一段时间,停止加热,冷却,停止通入N2.品红溶液不褪色。取下装置B,加入指示利.用0.2000moI/LNaOH溶液滴定剩余盐酸,终点时消耗NaOH溶液25.00mL,经检验滴定后的溶液中无SO42﹣。
(1)仪器X的名称是 .
(2)滴定前,下列操作的正确顺序是 (填字母编号).
a.盛装 0.2000mol/LNaOH溶液
b.用0.2000mol/L NaOH溶液润洗
c.读数、记录
d.查漏、清洗
e.排尽滴定尖嘴的气泡并调整液面
(3)装置B内溶液吸收气体的物质的量是 .
实验2:连接装置A﹣D﹣B,检查气密性.按图示重新加入试剂;通入N2排尽空气后,于400℃加热装置A至(NH4)2SO4完全分解无残留物。停止加热,冷却.停止通入N2,观察到装置A、D之间的导气管内有少量白色固体。经检验,该白色固体和装置D内溶液中有SO32﹣无SO42﹣。进一步研究发现,气体产物中无氮氧化物.
(4)检查装置D内溶液中有SO32﹣ 、无SO42﹣的实验操作和现象是 .
(5)装置B内溶液吸收的气体是 .
(6)(NH4)2SO4在400℃分解的化学方程式是 .
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省扶余市高一上学期第一次月考化学试卷(解析版) 题型:选择题
科学家已发现一种新型氢分子,其化学式为H3,在相同条件下,等质量的H3和H2相同的是
A.体积 B.分子数
C.原子数 D.物质的量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com