
【题目】下列说法中错误的是( )
A.质子数相同的原子,其核外电子排布也相同
B.质量数相同的原子,其化学性质一定相同
C.金属性越活泼,其原子在反应中越易失去电子
D.非金属性越活泼,其阴离子越难失去电子
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:
【题目】电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,电池总反应式为:Pb+PbO2+4H++2SO42﹣![]() 2PbSO4+2H2O则下列说法正确的是( )
2PbSO4+2H2O则下列说法正确的是( )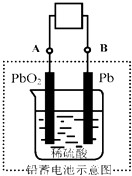
A.放电时:电子流动方向由A经导线流向B
B.放电时:正极反应是Pb﹣2e﹣+SO42﹣ ![]() PbSO4
PbSO4
C.充电时:铅蓄电池的负极应与充电器电源的正极相连
D.充电时:阳极反应是PbSO4﹣2e﹣+2H2O=PbO2+SO42﹣+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某“84 消毒液”瓶体部分标签如图所示,该“84 消毒液”通常稀释 100 倍(体积之比)后使用。请回答下列问题:

(1)该“84 消毒液”的物质的量浓度约为_________________mol·L-1。(保留两位有效数字)
(2)某同学取 100 mL 该“84 消毒液”,稀释后用于消毒,稀释后的溶液中 c(Na+)=________ mol·L-1。
(3)该同学参阅该“84 消毒液”的配方,欲用 NaClO 固体配制 250 mL含 NaClO 质量分数为 25%的消毒液。下列说法不正确的是______________(填序号)。
a.如图所示的仪器中,有三种是不需要的,还需要其它玻璃仪器
b.仪器E用蒸馏水洗净后,应烘干后才能用于溶液配制
c.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
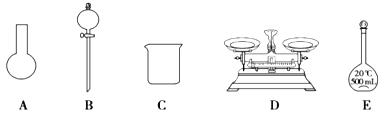
(4)仪器 E 使用前必须__________________。仪器 E上标记有________(填序号); ①质量 ②温度 ③刻度线 ④浓度 ⑤容积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述正确的是
A. 64g SO2中含有的原子数为3NA
B. 5.6g金属铁变为离子时失去的电子数为0. 3NA
C. 常温常压下,11.2L Cl2含有的分子数为0.5NA
D. 1mol/L NaOH溶液中Na+的数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《新修本草》是我国古代中药学著作之一,记载药物844种,其中有关于“青矾”的描述:“本来绿色,新出窟未见风者,正如琉璃……烧之赤色……”据此推测,“青矾”的主要成分为
A. FeSO4·7H2O B. CuSO4·5H2O
C. KAl(SO4)2·12H2O D. Fe2(SO4)3·9H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚砜(SOCl2)是一种液态化合物,沸点为 77℃,在农药、制药行业中用途广泛。SOCl2遇水剧烈反应,液面上产生白雾,并带有刺激性气味的气体产生.实验室合成原理:SO2+Cl2+SCl2═2SOCl2,部分装置如图所示,(已知 SCl2的沸点为 50℃).
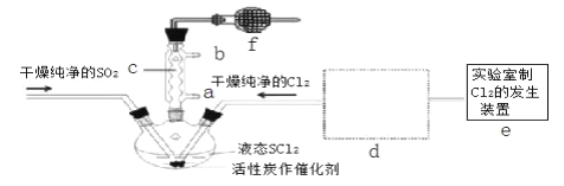
回答以下问题:
(1)下列四种制备 SO2的方案中最佳选择是____________________________
方案 | A | B | C | D |
发生装置 |
|
|
|
|
所选试剂 | 70%H2SO4+K2SO3 | 18.4mol/LH2SO4+Cu | 4mol/LHNO3+Na2SO3 | NaHCO3固体 |
(2)以 MnO2和浓盐酸为原料制备 Cl2的离子方程式为___________________________
(3)仪器 f 的作用是_________________________________________________
(4)d 的虚线框内隐含两个装置,按气流方向顺序这两个装置的药品分别是_______________。
(5)实验结束后,将三颈烧瓶混合物中产品分离出来的方法是 _________________________
(6)若用 SOCl2作 FeCl36H2O 的脱水剂,设计实验证明脱水时发生了氧化还原反应。取少量 FeCl36H2O 于试管中,加入过量 SOCl2,振荡,往试管中加水溶解,滴加____________或________溶液,证明脱水过程发生了氧化还原反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组学习化学反应速率后,联想到H2O2分解制备氧气,设计如下实验方案探究外界条件对反应速率的影响。
编号 | 温度 | 反应物 | 催化剂 |
甲 | 25℃ | 试管中加入3mL5%H2O2溶液 | 1mL蒸馏水 |
乙 | 25℃ | 试管中加入3mL5%H2O2溶液 | 1mL0.1mol/LFeCl3溶液 |
丙 | 40℃ | 试管中加入3mL5%H2O2溶液 | 1mL蒸馏水 |
(1)实验乙中发生反应的化学方程式为_______________。
(2)实验甲和实验乙的实验目的是____________。实验甲和实验丙的实验目的是___________。
(3)实验过程中该同学对实验乙中产生的气体进行收集,并在2min内6个时间点对注射器内气体进行读数,记录数据如下表。
时间/s | 20 | 40 | 60 | 80 | 100 | 120 | |
气体体积/mL | 实验乙 | 15.0 | 29.5 | 43.5 | 56.5 | 69.5 | |
0~20s的反应速率v1=__________mL/s,100~120s的反应速率v2=__________mL/s。不考虑实验测量误差,二者速率存在差异的主要原因是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com