
【题目】(1)AgNO3的水溶液呈_______(填“酸”“中”或“碱”)性,原因是(用离子方程式表示)________;实验室在配制AgNO3溶液时,常先将AgNO3固体溶于较浓的硝酸中,然后用蒸馏水稀释到所需的浓度,以_________________(填“促进”或“抑制”)其水解。
(2)明矾可用于净水,原因是(用离子方程式表示)_____________,把FeCl3溶液蒸干、灼烧,最后得到的主要固体产物是______________。
(3)泡沫灭火器的灭火原理是(用离子方程式表示)________________。
(4)纯碱可代替洗涤剂洗涤餐具,原因是(用离子方程式表示)_______________。
【答案】酸 Ag++H2O![]() AgOH+H+ 抑制 Al3++3H2O
AgOH+H+ 抑制 Al3++3H2O![]() Al(OH)3(胶体)+3H+ Fe2O3 Al3++3HCO3-=3CO2↑+Al(OH)3↓ CO32-+H2O
Al(OH)3(胶体)+3H+ Fe2O3 Al3++3HCO3-=3CO2↑+Al(OH)3↓ CO32-+H2O![]() HCO3-+OH-
HCO3-+OH-
【解析】
(1)Ag+对于的碱为AgOH,属于弱碱,故Ag+在水中会发生水解:Ag++H2O![]() AgOH+H+,导致溶液呈酸性,因Ag+在水中会发生水解,在配制AgNO3溶液时,故常先将AgNO3固体溶于较浓的硝酸中,增加溶液中H+浓度,从而抑制其水解,然后用蒸馏水稀释到所需的浓度,
AgOH+H+,导致溶液呈酸性,因Ag+在水中会发生水解,在配制AgNO3溶液时,故常先将AgNO3固体溶于较浓的硝酸中,增加溶液中H+浓度,从而抑制其水解,然后用蒸馏水稀释到所需的浓度,
故答案为:酸;Ag++H2O![]() AgOH+H+;抑制;
AgOH+H+;抑制;
(2)明矾净水的原理是利用Al3+水解生成Al(OH)3胶体,利用胶体吸附水中的杂质和悬浮颗粒,由Al3+水解生成Al(OH)3胶体的离子方程式为:Al3++3H2O![]() Al(OH)3(胶体)+3H+;FeCl3溶液蒸干过程中,Fe3+水解程度将会增加,溶液的酸度将会上升,盐酸浓度将会增加,因盐酸为易挥发性酸,故加热过程中,盐酸挥发使水解平衡正向移动,最终加热蒸干得到的固体为Fe(OH)3,然后将Fe(OH)3灼烧得到的固体为Fe2O3,
Al(OH)3(胶体)+3H+;FeCl3溶液蒸干过程中,Fe3+水解程度将会增加,溶液的酸度将会上升,盐酸浓度将会增加,因盐酸为易挥发性酸,故加热过程中,盐酸挥发使水解平衡正向移动,最终加热蒸干得到的固体为Fe(OH)3,然后将Fe(OH)3灼烧得到的固体为Fe2O3,
故答案为:Al3++3H2O![]() Al(OH)3(胶体)+3H+;Fe2O3;
Al(OH)3(胶体)+3H+;Fe2O3;
(3)泡沫灭火器灭火的原理是利用NaHCO3溶液与Al2(SO4)3溶液混合后发生强烈的相互促进双水解反应,生成二氧化碳气体、氢氧化铝固体,其离子方程式为:Al3++3HCO3-=3CO2↑+Al(OH)3↓,
故答案为:Al3++3HCO3-=3CO2↑+Al(OH)3↓;
(4)纯碱为碳酸钠,碳酸钠在溶液中会发生水解反应生成NaOH,NaOH可使油脂发生碱性水解生成醇和羧酸钠,从而达到去油污的效果,碳酸钠水解的离子方程式为:CO32-+H2O![]() HCO3-+OH-,
HCO3-+OH-,
故答案为:CO32-+H2O![]() HCO3-+OH-。
HCO3-+OH-。


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案科目:高中化学 来源: 题型:
【题目】某酸的酸式盐NaHY的水溶液中,HY-的电离程度小于HY-的水解程度,有关叙述中正确的是( )
A.H2Y在电离时为:H2Y+H2O![]() HY-+H3O+
HY-+H3O+
B.在该盐的溶液中,离子浓度为:c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+)
C.在该盐的溶液中,离子浓度为:c(Na+)>c(HY-)>c(Y2-)>c(OH-)>c(H+)
D.HY-的水解方程式为:HY-+H2O![]() H3O++Y2-
H3O++Y2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D为由短周期元素组成的四种物质,它们有如下所示转化关系,且D为强电解质(其他相关物质可能省略)。
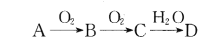
下列说法不正确的是
A. 若A为非金属单质,则它与Mg反应的产物中阴、阳离子个数比可能为2:3
B. 若A为非金属单质,则其组成元素在周期表中的位置可能处于第二周期第IVA族
C. 若A是共价化合物,则A和D有可能发生氧化还原反应
D. 若A是金属或非金属单质,则常温下0. 1 mol/L的D溶液中由水电离出的c(H+)可能为10-13mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在中学化学实验中研究和推广微量化实验符合绿色化学原则。下列对微量化实验装置图的解读不正确的是( )
A.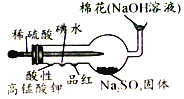 二氧化硫性质的组合实验装置。将稀硫酸挤入干燥管胖肚中,则前端小凹槽内三种溶液均能褪色。
二氧化硫性质的组合实验装置。将稀硫酸挤入干燥管胖肚中,则前端小凹槽内三种溶液均能褪色。
B.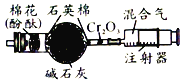 氨的催化合成装置。将注射器内的氮气和氢气缓缓通过加热的催化剂,即可观察到蘸有酚酞溶液的棉团变红。
氨的催化合成装置。将注射器内的氮气和氢气缓缓通过加热的催化剂,即可观察到蘸有酚酞溶液的棉团变红。
C.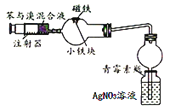 苯与液溴反应的装置。反应发生后,青霉素小瓶中产生黄色沉淀,证明该反应为取代反应。
苯与液溴反应的装置。反应发生后,青霉素小瓶中产生黄色沉淀,证明该反应为取代反应。
D.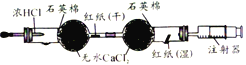 氯气的制备与漂白装置。前端凹槽内放入高锰酸钾固体,滴入浓盐酸后,干燥的红纸不退色,湿润的红纸退色。
氯气的制备与漂白装置。前端凹槽内放入高锰酸钾固体,滴入浓盐酸后,干燥的红纸不退色,湿润的红纸退色。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取一支硬质大试管,通过排饱和食盐水的方法先后收集半试管甲烷和半试管氯气(如图),下列说法正确的是( )
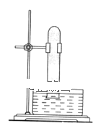
A.此反应无光照也可发生
B.甲烷和Cl2反应后的产物只有CH3Cl和HCl
C.盛放饱和食盐水的水槽底部会有少量晶体析出
D.CH4和Cl2完全反应后液面上升,液体充满试管
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t℃时,Ag2CrO4(橘红色)在水溶液中的沉淀溶解平衡曲线如图所示。又知AgCl的Ksp=1.8×10-10。下列说法不正确的是
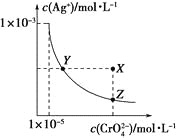
A.t ℃时,Ag2CrO4的Ksp为1×10-11
B.饱和Ag2CrO4溶液中加入K2CrO4能使溶液由Y点变为X点
C.t ℃时,Y点和Z点时Ag2CrO4的Ksp相等
D.t ℃时,将0.01mol·L-1AgNO3溶液滴入20mL0.01mol·L-1KCl和0.01mol·L-1K2CrO4的混合溶液中,Cl-先沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验结论与实验操作及现象不相符的一组是( )
选项 | 实验操作及现象 | 实验结论 |
A | 向某酸雨样品中加入Ba(OH)2溶液,有白色沉淀生成 | 酸雨试样中一定含SO42- |
B | 向KI-淀粉溶液中滴入氯水,溶液变成蓝色 | I-的还原性强于Cl- |
C | 将Ba(OH)2·8H2O和NH4Cl晶体在小烧杯中混合搅拌,用手触摸烧杯外壁感觉变凉 | Ba(OH)2·8H2O与NH4Cl的反应是吸热反应 |
D | 向某盐溶液中加入NaOH溶液,加热,用湿润的红色石蕊试纸放在试管口,试纸变蓝 | 该盐溶液中含有NH4+ |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生态工业园区的建设,不仅仅是体现环保理念,重要依据循环经济理论和充分考虑经济的可持续发展,如图是某企业设计的硫酸-磷铵-水泥联产,海水-淡水多用,盐-热-电联产生三大生态产业链流程图。根据上述产业流程回答下列问题:

(1)从原料、能源、交通角度考虑该企业应建在______
A西部山区 B沿海地区 C发达城市 D东北内陆
(2)该流程①、②、③、④、⑤为能量或物质的输送,请分别写出输送的主要物质的化学式或能量形式:①______、②______、③______、④______、⑤______。
(3)沸腾炉发生反应的化学方程式:______;磷肥厂的主要产品是普钙,其主要成分是______(填化学式)。
(4)热电厂的冷却水是______,该流程中浓缩盐水除提取盐以外还可提取的物质有______(写出一种即可)。
(5)根据现代化工厂没计理念请提出高炉炼铁厂废气、废渣及多余热能的利用设想。______,______(写出两点即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com