
�����ұ��ṩ�����ݣ������ж���ȷ���ǣ�������
|



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ұ��ṩ�����ݣ��ж��ڵ�Ũ�ȵ�![]() ��
��![]() �����Һ�У���������Ũ�ȹ�ϵ��ȷ����
�����Һ�У���������Ũ�ȹ�ϵ��ȷ����
![]()

A��![]()
![]() B��
B��![]()
![]() C��
C��![]()
![]() D��
D��![]()
![]()
![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ��ɽ��ʡ��������ˮһ�и߶�12��������⻯ѧ�Ծ����������� ���ͣ���ѡ��
�����ұ��ṩ�����ݣ��ж��ڵ�Ũ�ȵ� ��
�� �����Һ�У���������Ũ�ȹ�ϵ��ȷ���� �� ��
�����Һ�У���������Ũ�ȹ�ϵ��ȷ���� �� ��
A�� |
B�� |
C�� |
D�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ���㽭ʡ�����и�����ѧ�ڻ������Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ұ��ṩ�����ݣ������ж���ȷ����

A��ͬ��ͬŨ���£���Һ��
B�����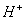 H+��������
H+��������
C��̼������Һ�м����������������ӷ���ʽ��
D������������Һ��ͨ����������̼�����ӷ���ʽ��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��ɽ��ʡ�����и߶�12��������⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ұ��ṩ�����ݣ��ж��ڵ�Ũ�ȵ� ��
�� �����Һ�У���������Ũ�ȹ�ϵ��ȷ����
��
��
�����Һ�У���������Ũ�ȹ�ϵ��ȷ����
��
��

A.
B.
C.
D.
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com