

| ��ɫ��״̬ | �е㣨�棩 | �ܶȣ�g•cm-3�� | |
| ������* | ��ɫ��Ƭ״���� | 249 | 1.2659 |
| ���������� | ��ɫ����Һ�� | 212.6 | 1.05 |
| �Ҵ� | ��ɫ����Һ�� | 78.3 | 0.7893 |
| ������ | ��ɫ����Һ�� | 80.8 | 0.7318 |
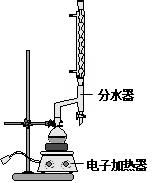
���� ��1�������������ܴٽ�ƽ��������Ӧ�����ƶ���
��2�����ݷ�ˮ����ˮλ�жϣ�
��3���¶ȵ��ڱ����������ķе�ʱ�����������������������Ҫʹ������������������������¶�Ӧ���ڱ����������ķе㣬�����¶�Ӧ����212.6�棬��Ҫʹ�Ҵ��ͻ�����������������¶�Ӧ�����Ҵ��ͻ�����ķе㣻
��4�������ǹ���С��������Ϊ��������100���Ѹ�����������Կ����DZ����������л���δ�����ı����
��5������©����ʹ�÷��������뽫ˮ��Һ�м������ѣ�ת������Һ©���У����ϲ�����������Һ©����ת������������ҡ�����ҷų�Һ��ʱ���轫�������ϵİ��۶�©�����ϵ�С�ף�ֻ������Һ�����˳�����£�
��6������ʱ���õIJ��������оƾ��ơ������ܡ�����������ƿ��������ƿ���¶ȼƣ��ɴ˷������
��7��ʵ��IJ���=$\frac{ʵ�ʲ���}{���۲���}$��100%��
��� �⣺��1����Ӧ Ϊ���淴Ӧ������������ˮ���ɣ��������ʹ�÷�ˮ�����Ϸ����ȥˮ������ʹ�������Ũ�ȼ�С����ѧƽ�����������ƶ����Ӷ������˲��ʣ�
Ϊ���淴Ӧ������������ˮ���ɣ��������ʹ�÷�ˮ�����Ϸ����ȥˮ������ʹ�������Ũ�ȼ�С����ѧƽ�����������ƶ����Ӷ������˲��ʣ�
�ʴ�Ϊ��ʹƽ�ⲻ�ϵ��������ƶ����Ӷ���߲�Ʒ���ʣ�
��2�����÷�Ӧ��ɺͲ�������ˮ������Ȼ�������ˮ����ˮλ�����������ʴ�Ϊ����ˮ���е�ˮ�㲻������ʱ����Ϊ��Ӧ���յ㣻
��3���¶ȵ��ڱ����������ķе�ʱ�����������������������Ҫʹ������������������������¶�Ӧ���ڱ����������ķе㣬�����¶�Ӧ����212.6�棬��Ҫʹ�Ҵ��ͻ�����������������¶�Ӧ�����Ҵ��ͻ�����ķе�80.8���ʴ�Ϊ��C��
��4�������ǹ���С��������Ϊ��������100���Ѹ�����������Կ����DZ����������л���δ�����ı����ᣬ���������������̣��ʴ�Ϊ�������������л���δ�����ı����ᣬ��������100��ʱ����������
��5������©����ʹ�÷��������뽫ˮ��Һ�м������ѣ�ת������Һ©���У����ϲ�����������Һ©����ת������������ҡ�����ҷų�Һ��ʱ���轫�������ϵİ��۶�©�����ϵ�С�ף�ֻ������Һ�����˳�����£���ѡ��A D��
��6������ʱ���õIJ��������оƾ��ơ������ܡ�����������ƿ��������ƿ���¶ȼƣ��ʴ�Ϊ��������ƿ���¶ȼƣ�
��7��12.20g����������ʵ���Ϊ��$\frac{12.20g}{122g/mol}$=0.1mol�������ɱ���������������Ϊ��12.86mL��1.05g•ml-1=13.503g�����ʵ���Ϊ��$\frac{13.503g}{122g/mol}$=0.11mol������ʵ��IJ���=$\frac{ʵ�ʲ���}{���۲���}$��100%=$\frac{0.1}{0.11}$��100%=90%���ʴ�Ϊ��90%��
���� ���⿼�������Ʊ���Ϊ��Ƶ���㣬�漰���㡢������ѡȡ�����ʷ�����ᴿ��֪ʶ�㣬��ȷʵ��ԭ���ǽⱾ��ؼ���ע�ⷴӦ�������жϱ�־����Ŀ����ӱ��Ϊ�״��⣮


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
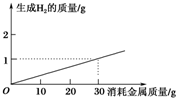
| A�� | ��п | B�� | ���� | C�� | þ���Ͻ� | D�� | ͭ���Ͻ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
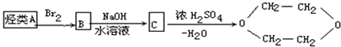
| A�� | ��ϩ | B�� | �Ҵ� | C�� | �Ҷ��� | D�� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
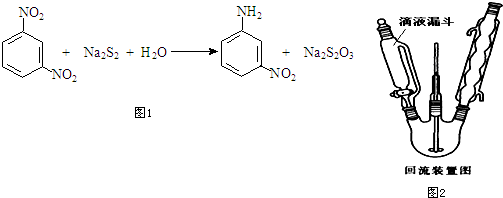
 �����������ڽ����ơ�������Ͷ����ƣ�Na2Sx���ֱ���Ϊ�����缫�ķ�Ӧ�����Al2O3�մɣ��ɴ���Na+��Ϊ����ʣ��䷴Ӧԭ����ͼ��ʾ��
�����������ڽ����ơ�������Ͷ����ƣ�Na2Sx���ֱ���Ϊ�����缫�ķ�Ӧ�����Al2O3�մɣ��ɴ���Na+��Ϊ����ʣ��䷴Ӧԭ����ͼ��ʾ��| ���� | Na | S | Al2O3 |
| �۵�/�� | 97.8 | 115 | 2050 |
| �е�/�� | 892 | 444.6 | 2980 |
| A�� | �ŵ�ʱ���缫AΪ���� | |
| B�� | �����ϱ����ݣ������жϸõ�ع����������¶�Ӧ������350�桫2050�� | |
| C�� | �ŵ�ʱ��Na+���ƶ�����Ϊ�ӵ缫A���缫B | |
| D�� | ���ʱ���ܷ�ӦΪNa2Sx�T2Na+xS��3��x��5�����������ĵ缫��ӦʽΪSx2--2e-�TxS |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������������ʵ���Ũ�ȵ�HA��HAΪ���ᣩ��NaA��ϣ����û��Һ�������ȡ����Ka��HA���Ĵ�С | |
| B�� | CH3COOH ��Һ��ˮϡ�ͺ���Һ��c��H+��/c��CH3COO-�� ��ֵ��С | |
| C�� | ij��ˮ��pH=a��ij�����pH=b����֪a+b=14����������ˮ������������Ϻ���Һ�и�������Ũ�ȵĹ�ϵΪc��NH4+����c��Cl-����c��OH-����c��H+�� | |
| D�� | �����ʵ�����NaClO��NaHCO3�����Һ�У�c��HClO��+c��ClO-���Tc��HCO3-��+c��H2CO3��+c��CO32-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
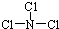 ��X ��ˮ��Ӧ�Ļ�ѧ����ʽ��NCl3+3H2O�TNH3+3HClO��
��X ��ˮ��Ӧ�Ļ�ѧ����ʽ��NCl3+3H2O�TNH3+3HClO���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ƼغϽ�����������ӷ�Ӧ�ѵ��ȼ���ԭ��֮һ�dz����³�Һ̬ | |
| B�� | �ҹ�����Ա���ĺ����ʹ�õĸ�ǿ�ȡ������Ե�������������һ���л��߷��Ӻϳɲ��� | |
| C�� | ����Ҫ�Ե��ʡ�����������ε���ʽ��������Ȼ���� | |
| D�� | ����������ȼ�ϣ���ȼ�ϵ�����������ϳɿ������Ĵ�����ϣ�����ʵ�������ġ����ŷš� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com