
| A. | 容器内压强 | B. | 平均相对分子质量 | ||
| C. | 各组分浓度 | D. | 混合气体的颜色 |
分析 反应2HI(g)?H2(g)+I2(g),反应前后气体的化学计量数之和相等,反应前后气体的物质的量不变,当达到化学平衡时,正逆反应速率相等,各物质的浓度不变,混合气体的颜色不变.
解答 解:A.反应前后气体的化学计量数之和相等,反应前后气体的物质的量不变,容器内的压强不变,不能作为判断是否达到化学平衡的依据,故A错误;
B.反应前后气体的物质的量不变,质量不变,则平均相对分子质量不变,不能作为判断是否达到化学平衡的依据,故B错误;
C.各成分浓度不随时间变化,说明正逆反应速率相等,达化学平衡的依据,故C正确;
D.当达到化学平衡时,正逆反应速率相等,各物质的浓度不变,混合气体的颜色不变,故D正确.
故选CD.
点评 本题考查化学平衡状态的判断,题目难度不大,注意反应前后气体的化学计量数之和相等,反应前后气体的物质的量不变,平均相对分子质量不变,不能作为判断的依据.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 4.6g | B. | 4.1g | C. | 6.9 g | D. | 9.2g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯能使酸性高锰酸钾溶液褪色,而甲烷不能使酸性高锰酸钾溶液褪色 | |
| B. | 乙基对羟基的影响,使羟基的活性变弱,电离H+的能力不及H2O | |
| C. | 相等物质的量的甘油和乙醇分别与足量金属钠反应,甘油产生的H2多 | |
| D. | 苯酚中的羟基氢能与NaOH溶液反应,而醇羟基氢不能与NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
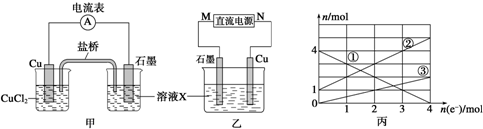
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热这两种固体物质,并将生成的气体通入澄清的石灰水中 | |
| B. | 在这两种物质的溶液中加入CaCl2溶液 | |
| C. | 在等物质的量浓度的两种物质的溶液中分别滴加稀盐酸 | |
| D. | 在这两种物质的溶液中加入少量澄清的石灰水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用小苏打治疗胃酸过多:2H++CO32-═H2O+CO2↑ | |
| B. | 氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| C. | 向NaHSO4溶液中滴加Ba(OH)2溶液至恰好为中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O | |
| D. | 碳酸氢钠溶液与过量的氢氧化钙溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com