
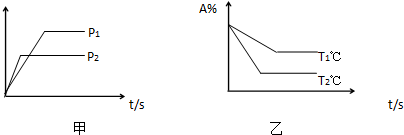
| A、温度T1℃比 T2℃高 |
| B、正反应为放热反应 |
| C、甲图纵轴可以表示A的转化率 |
| D、甲图纵轴可以表示混合气体平均相对分子质量 |


科目:高中化学 来源: 题型:
| A、Na+、Mg2+、SO42-、Cl- |
| B、Na+、Ca2+、CO32-、NO3- |
| C、Na+、H+、Cl-、CO32- |
| D、K+、Fe3+、SO42-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.8 a g |
| B、1.6a g |
| C、(a-0.8)g |
| D、(a-1.6)g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 弱酸 | HA | HB | H2C |
| 电离平衡常数 (25℃) | K=1.77×10-4 | K=4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A、2Bˉ+H2C=2HB+C2- |
| B、2HA+C2-=2Aˉ+H2C |
| C、中和等体积、等pH的HA和HB消耗NaOH的量前者小于后者 |
| D、等体积、等浓度的NaA和NaB溶液中所含离子总数前者大于后者 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |
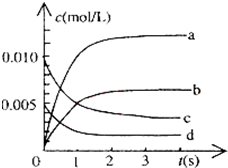
| n(NO2) |
| n(NO) |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示,两个连通容器用活塞分开,左右两室(体积相同)各充入一定量NO和O2,且恰好使两容器内气体密度相同.打开活塞,使NO与O2充分反应.(已知2NO+O2═2NO2)
如图所示,两个连通容器用活塞分开,左右两室(体积相同)各充入一定量NO和O2,且恰好使两容器内气体密度相同.打开活塞,使NO与O2充分反应.(已知2NO+O2═2NO2)查看答案和解析>>
科目:高中化学 来源: 题型:
| A、50mL 12 mol?L-1浓盐酸与足量二氧化锰加热反应,转移电子数为0.3 NA |
| B、5.6 g铁与0.1 mol氯气充分反应转移电子数为0.3NA |
| C、1L1mol?L-1NaClO溶液中含有ClO-的数目为NA |
| D、60gSiO2晶体中含有硅氧键的数目为4 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com