(2009?静安区二模)利用化工厂生产硼砂的废渣--硼镁泥可制取七水硫酸镁(MgSO
4?7H
2O),硼镁泥的主要成分是MgCO
3,还含有其它杂质(MgO、SiO
2、Fe
2O
3、FeO、CaO、Al
2O
3、MnO等).
表1 部分阳离子以氢氧化物形式完全沉淀时溶液的pH
| 沉淀物 |
Al(OH)3 |
Fe(OH)3 |
Fe(OH)2 |
Mn(OH)2 |
Mg(OH)2 |
| pH值 |
5.2 |
3.2 |
9.7 |
10.4 |
11.2 |
表2 两种盐的溶解度(g/100g水)
| 温度/℃ |
10 |
30 |
40 |
50 |
60 |
| CaSO4 |
0.19 |
0.21 |
0.21 |
0.20 |
0.19 |
| MgSO4?7H2O |
30.9 |
35.5 |
40.8 |
45.6 |
/ |
硼镁泥制取七水硫酸镁的工艺流程如下:
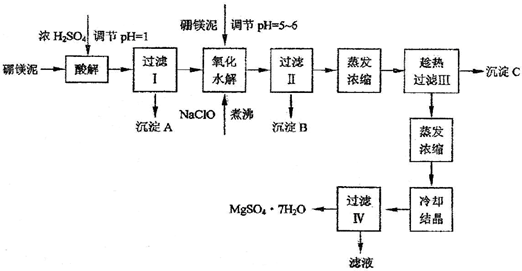
根据以上流程图并参考pH数据和溶解度数据,试回答下列问题:
(1)硼镁泥加入浓硫酸时,FeO发生的变化是
bc
bc
(选填序号).
a.被钝化 b.被氧化 c.被溶解
(2)往过滤Ⅰ得到的滤液中加入硼镁泥,调节溶液的pH=5~6,再加入NaClO溶液可将溶液中的Mn
2+氧化成MnO
2,该反应的离子反应方程式为
Mn2++ClO-+H2O═MnO2↓+2H++Cl-
Mn2++ClO-+H2O═MnO2↓+2H++Cl-
.加热煮沸的目的是
促进Al3+、Fe3+水解
促进Al3+、Fe3+水解
.
(3)沉淀B中除MnO
2外还含有
Fe(OH)3、Al(OH)3
Fe(OH)3、Al(OH)3
(填化学式)等物质.
(4)沉淀C的化学式是
CaSO4?2H2O或CaSO4
CaSO4?2H2O或CaSO4
;产生沉淀C的操作需趁热进行的原因是
以防MgSO4在温度低时结晶析出
以防MgSO4在温度低时结晶析出
;洗涤沉淀需要的玻璃仪器有:烧杯、
漏斗、玻璃棒
漏斗、玻璃棒
;若用乙醇代替水作洗涤剂洗涤沉淀C,原因是
降低CaSO4?2H2O的溶解度(或减少CaSO4?2H2O的溶解)
降低CaSO4?2H2O的溶解度(或减少CaSO4?2H2O的溶解)
.
(5)过滤出MgSO
4?7H
2O晶体的滤液中含有的金属阳离子有
Mg2+、Na+
Mg2+、Na+
,生产中对该滤液的处理方法是
循环利用
循环利用
;检验滤液是否含有SO
42-操作是
取滤液1~2mL于试管中,加入BaCl2溶液,若有白色沉淀生成,说明有SO42-.
取滤液1~2mL于试管中,加入BaCl2溶液,若有白色沉淀生成,说明有SO42-.
.



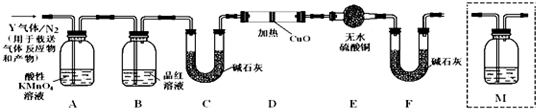

 目前工业上有一种方法是用CO2来生产燃料甲醇.CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,为探究反应原理,现进行如下实验:
目前工业上有一种方法是用CO2来生产燃料甲醇.CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,为探究反应原理,现进行如下实验: