
分析 (1)煤的汽化是煤和水蒸气反应生成CO和氢气;将煤隔绝空气加强热使煤分解的操作是煤的干馏;
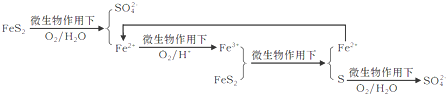
(2)①根据微生物脱硫技术的原理来分析;Fe2+做还原剂,被氧气氧化为Fe3+,氧气在酸性条件下被还原为H2O,据此写出离子方程式;
②在煤燃烧的同时进行的脱硫技术称为“流化床”燃烧技术;根据SO2是酸性氧化物来分析;
③吸收烟气的装置为吸收塔.
解答 解:(1)煤的汽化是煤和水蒸气在高温条件下反应生成CO和氢气的过程,故主要产物为CO、H2;将煤隔绝空气加强热使煤分解得到焦炉气、煤焦油及焦炭等产品的操作是煤的干馏,故答案为:CO、H2;煤的干馏;
(2)①根据微生物脱硫技术的原理可知:Fe2+先被氧化为Fe3+,后Fe3+又被还原为Fe2+,即Fe2+先被消耗后又生成,故在反应中做催化剂;Fe2+做还原剂,被氧气氧化为Fe3+,氧气在酸性条件下被还原为H2O,据此写出离子方程式:4Fe2++O2+4H+=4Fe3++2H2O,
故答案为:中间产物,催化剂作用,加快S元素的氧化;4Fe2++O2+4H+=4Fe3++2H2O;
②在煤燃烧的同时进行的脱硫技术称为“流化床”燃烧技术;由于SO2是酸性氧化物,故可以加碱性氧化物CaO(或者CaCO3)来加以吸收,故答案为:流化床;CaO(或者CaCO3);
③吸收烟气的装置为吸收塔,故答案为:吸收塔.
点评 本题考查二氧化硫的污染及治理,题目难度中等,本题注意从题目中获取信息,结合物质的性质解答.


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 被提纯的物质 | 选用试剂 | 操作方法 |
| A | CaO(CaCO3) | 水 | 溶解、过滤、结晶 |
| B | CuSO4(H2SO4) | NaOH溶液 | 过滤 |
| C | CO2(CO) | 氧气 | 点燃 |
| D | Cu(CuO) | 稀盐酸 | 溶解、过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 减小C 或D 的浓度 | B. | 增大压强 | ||
| C. | 减小B 的浓度 | D. | 增大 A 或B的浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 呵护生存环境,共建和谐社会.
呵护生存环境,共建和谐社会.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 氮化铝中氮元素的化合价为-3 | |
| B. | 上述反应中每生成2molAlN,N2得到3mol电子 | |
| C. | 在氮化铝的合成反应中,N2是氧化剂,Al2O3是还原剂 | |
| D. | 该反应不属于四种基本反应类型中任一种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | M可能为铜,X可能为氯化铁 | B. | M可能为石墨,Y可能为硫酸铁 | ||
| C. | 电子由铁经盐桥流向M极 | D. | 盐桥中K+向铁极迁移 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HSO4-、Na+、OH-、K+ | B. | HCO3-、NO3-、Mg2+、Ba2+ | ||
| C. | Ba2+、Mg2+、NO3-、Cl- | D. | Mg2+、Na+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com