
| A. | pH=1的无色溶液:Na+、Cu2+、NO3-、SO42- | |
| B. | 能溶解Al(OH)3固体的溶液:K+、Na+、HCO3-、SO42- | |
| C. | 水电离出的c(H+)=10-12mol/L的溶液:Ba2+、Na+、Cl-、NO3- | |
| D. | 能使淀粉KI试纸变蓝的溶液:K+、Fe2+、NO3-、Cl- |
分析 A.pH=1的溶液中存在大量氢离子,无色溶液中不存在有色的铜离子;
B.能溶解Al(OH)3固体的溶液为强碱溶液或酸性溶液,碳酸氢根离子与氢离子、氢氧根离子反应;
C.水电离出的c(H+)=10-12mol/L的溶液为酸性或碱性溶液,四种离子之间不反应,都不与氢离子和氢氧根离子反应;
D.能使淀粉KI试纸变蓝的溶液具有氧化性,亚铁离子具有还原性.
解答 解:A.Cu2+为有色离子,不满足溶液无色的条件,故A错误;
B.能溶解Al(OH)3固体的溶液中存在大量氢离子或氢氧根离子,HCO3-与氢离子和氢氧根离子反应,在溶液中一定不能大量共存,故B错误;
C.水电离出的c(H+)=10-12mol/L的溶液中存在大量氢离子或氢氧根离子,Ba2+、Na+、Cl-、NO3-之间不发生反应,都不与氢离子、氢氧根离子反应,在溶液中能够大量共存,故C正确;
D.能使淀粉KI试纸变蓝的溶液具有氧化性,能够氧化Fe2+,在溶液中不能大量共存,故D错误;
故选C.
点评 本题考查离子共存的判断,为高考的高频题,题目难度中等,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”等.


科目:高中化学 来源: 题型:选择题
| A. | 反应①中的氧化剂Cl2,氧化产物是KCl | |
| B. | 氧化性由强到弱顺序为 Cl2>KClO3>Br2 | |
| C. | 反应③中的HNO3体现了酸性和氧化性 | |
| D. | 反应③中有0.4mol HNO3参加反应时,转移电子物质的量为0.4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
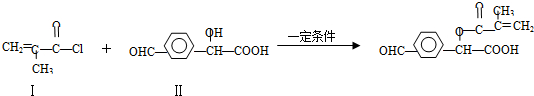
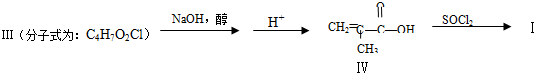
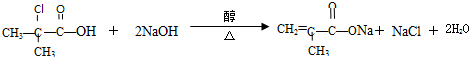 .
.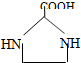 与足量的化合物Ⅰ在一定条件下也能发生类似反应①的反应,生成有机化合物Ⅵ,则Ⅵ的结构简式为
与足量的化合物Ⅰ在一定条件下也能发生类似反应①的反应,生成有机化合物Ⅵ,则Ⅵ的结构简式为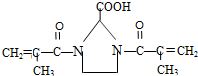 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在常温常压下,2.24L SO2与O2混合气体中所含氧原子数为0.2NA | |
| B. | 标准状况下,20g D2O分子中所含中子数为10NA | |
| C. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA | |
| D. | 50mL 12mol•L-1盐酸与足量MnO2共热,转移的电子数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
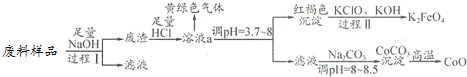
| 温度范围(℃) | 固体质量(g) |
| 150-210 | 4.41 |
| 290-320 | 2.41 |
| 890-920 | 2.25 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg2+ Na+ OH- | B. | Al3+ NO3- Cl- | ||
| C. | K+ H+ HCO3- | D. | Mg2+ Ca2+ SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 干冰汽化需吸收大量的热,这个变化是吸热反应 | |
| B. | 浓硫酸溶于水会放出大量热,这属于放热反应 | |
| C. | 用氢氧焰可以加热软化玻璃制玻璃器皿,这利用了氢气和氧气化合时放出的热量 | |
| D. | 木炭需加热到一定温度时才燃烧,所以木炭燃烧是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
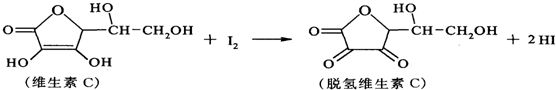
| A. | 上述反应为氧化还原反应 | |
| B. | 维生素C分子中有3种官能团 | |
| C. | 脱氢维生素C不能与氢气发生加成反应 | |
| D. | 脱氢维生素C的分子式为C6H6O6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com