
��һ��ϡ��Һ�������������֣���Һ��ɫ�����壬���п��ܺ���SO42����Na+��CO32����H+��NO3����HCO3����Cl�� �������е������֣�Ȼ������������ʵ�飬��ȷ����Щ�����Ƿ�������ڣ�
����ʯ����ֽ����Һ������ԣ���ֽ�Ժ�ɫ��
��ȡ2������Һ�����Ȼ�����ϡ������м��飬��������˰�ɫ������
�۶Ԣ������û���ᄇ�ú�ȡ�ϲ���ҹ����������Һ��ϡ������飬����������˰�ɫ�������Իش��������⣺
��1��ԭ��Һ��һ�����ڵ������� ��һ�������ڵ������� ��
��2������ʵ������У��д���IJ����ǣ���д���ţ� ���Դ���ĸ��������� ��
��3��������������ʵ�飬�����ܿ϶��Ƿ���ڵ������� ��
��4��д���ڡ��۲���Ӧ�����ӷ���ʽ���� ���� ��
 �ִʾ��ƪϵ�д�
�ִʾ��ƪϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ��һ12���¿���ѧ�Ծ��������棩 ���ͣ��ƶ���
A��B��C��D��F�������ʵ���ɫ��Ӧ��Ϊ��ɫ��A��B��C��D�����ᷴӦ������E������B������һ�ֿ�ȼ���壬C��D������һ����ɫ��ζ����H����������ʹ����ʯ��ˮ����ǣ�D��A�ɷ�Ӧ����C��F��HҲ�ɷ�Ӧ����C����һ����ɫ��ζ���壮��ش��������⣺
��1��д�������ʵĻ�ѧʽ��A___________��B ____________��C_______
��2��д��F��H��Ӧ�Ļ�ѧ����ʽ______________________________��
��3��д�����з�Ӧ�����ӷ���ʽ��
��D+����______________________________��
��B+ˮ______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ӱ�ʡ������ѧ�ڵ��Ĵε��л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NAΪ�����ӵ�����������˵���в���ȷ���ǣ� ��
A����״���£��ܶ�Ϊdg/L��ij���崿����һ�����ӵ�����Ϊ22.4d/NAg
B�����������£�20mL10mol/L��Ũ����������ͭ��Ӧת�Ƶ�����Ϊ0.1NA
C����⾫��ͭ�Ĺ�����ת����NA�����ӣ�����������32gͭ
D��1L pH=1��������Һ�У�����0.1NA��H+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʡ������ѧ��12���ʼ컯ѧ�Ծ��������棩 ���ͣ�ѡ����
ij��ȤС�������ͼ��ʾ����ʵ��װ�ã�ʵ��ʱ���ȶϿ�K2���պ�K1�������������ݲ�����һ��ʱ��Ͽ�K1���պ�K2�����ֵ�����ָ��ƫת�������й�������ȷ����
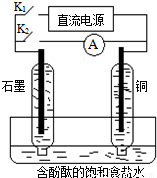
A���Ͽ�K2���պ�K1ʱ���ܷ�Ӧ�����ӷ���ʽΪ��2H++2Cl- Cl2��+H2��
Cl2��+H2��
B���Ͽ�K2���պ�K1ʱ��ͭ�缫������Һ���
C���Ͽ�K1���պ�K2ʱ��ͭ�缫�ϵĵ缫��ӦΪ��Cl2+2e-=2Cl-
D���Ͽ�K1���պ�K2ʱ��ʯī�缫������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�갲��ʡ�߶������в��Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
��ˮ�к��зḻ�Ļ�ѧԪ�أ�������ij�������Ӻ�ˮ����ȡNaCl��Mg(��MgCl2��ʽ����)��Br2(��NaBr����ʽ����)���ۺ����õ��������̼�ͼ��

��ش�
��1���ڴ����к���Ca2+��Mg2+��SO42-�����ʣ�����ʱ���õ��Լ�Ϊ��
A������ B���Ȼ�����Һ C������������Һ D��̼������Һ
������Լ���˳����(����) ��
��2��Mg(OH) 2�м��������Ҫ���MgCl 2•6H 2O���壬��Ҫ���е�ʵ��������� ��
A������ B������ C������ D������ E����ȴ�ᾧ
��3��Ŀǰ��ҵ����Ҫ�������ӽ���Ĥ����ⱥ��ʳ��ˮ�����й������ӽ���Ĥ���۵������������ ��
A�����Ʊ���ʳ��ˮ���������� B����ˮ(������NaOH)����������
C����������Ϊ�������ƺ����� D�����۵������ý��������Ƴ�
��4��д����ⱥ��NaCl��Һ�����ӷ���ʽ��
��5�� ����MgCl 2•6H 2O���Ƶ���ˮ�Ȼ�þ��Ӧ��ȡ�Ĵ�ʩ��
��6�� ���ȿ�������������������������������Һ���գ�д����Ӧ�Ļ�ѧ����ʽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�갲��ʡ��һ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���и��������У�����������ʡ������˳�����е�һ���ǣ� ��
A���ռҺ̬������� B����ʯ�ҡ����ס���ʯ��
C���ɱ��������Ȼ��� D������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��㶫��ͷ��ɽ��ѧ��һ��12���¿���ѧ���������棩 ���ͣ������
д�����й�����������Ӧ�����ӷ���ʽ
��1����400 mL 0.5 mol��L-1��NaOH��Һ����8.96 g SO2���壺 ��
��2������������Ͷ��NaOH��Һ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ�߶��϶������Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ˮ���������H+Ũ��Ϊ1��10-13mol��L-1����Һ�У�һ���ܴ����������������
��K+��Cl-��NO3-��S2- ��K+��Fe3+��I-��SO42-
��Na+��Cl-��NO3-��SO42- ��Na+��Ca2+��Cl-��HCO3- ��K+��Ba2+��Cl-��NO3-
A���٢� B���ۢ� C���ۢ� D���ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������и�һ�����в��Ի�ѧ�Ծ��������棩 ���ͣ��ƶ���
����һ����ɫ��Һ��ֻ������Na+��Cl-��H+��SO42-��CO32-��Cu2+��NO3-�еļ��֣�����ˮ�������������OH-����ȡ����Һ��⣬������Һ��ǿ���ԡ�
��1������Ҫ��һ��ʵ�飬�����жϣ���Һ��һ������________��һ��������__________��
��2����һ���ⶨ�����ָ���Һ��c(H+)=0.1mol/L��ȡ100mL����Һ����������BaCl2������2.33g���������ˣ���Һ�м�������AgNO3��Һ������5.74g������100mL��Һ���Ƿ���Cl��______����һ���С�һ��û�С������У���100mL��Һ��Na+�����ʵ���Ũ������Ϊ_______mol/L��
������������ˮ����������A��B��C��D��E��������һ���Ǽ�������Σ�����ˮ�������Բ����±��е����ӣ�
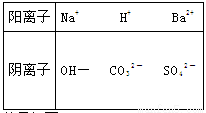
Ϊ�������ǣ��ֱ��������ʵ�飬�������£�
��A��Һ��B��Һ��Ӧ������ɫ����X������X���Ժ�C��Һ��Ӧ���ɳ���E������E����B��Һ��Ӧ��
��B��Һ��C��Һ��Ӧ���ɰ�ɫ����D������D������ϡ���ᣮ
���������ʵ��������գ�
��1��д���������ʵĻ�ѧʽ��X__________��C__________��B__________
��2�����A��Һ��X���巴Ӧ�����ӷ���ʽ��__________
��3��D��E�Ļ����ag�������������ᣬ��Ӧ������ɱ�״��ʱ������bL����D�ڻ�����е���������Ϊ_____________��
��4����֪NaHCO3��Һ�ʼ��ԣ�B��Һ��A��Һ��Ӧ��ǡ����Һ�����ԣ�д���ù��̵����ӷ���ʽ_________
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com