
| A、3:2:1 |
| B、1:2:3 |
| C、1:1:1 |
| D、2:3:1 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
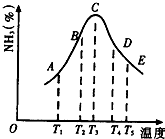 (1)在容积不同的密闭容器内,分别充入同量的N2和H2,在不同温度下,任其发生反应N2+3H2?2NH3,并分别在t秒时测定其中NH3的体积分数,绘图如图所示:
(1)在容积不同的密闭容器内,分别充入同量的N2和H2,在不同温度下,任其发生反应N2+3H2?2NH3,并分别在t秒时测定其中NH3的体积分数,绘图如图所示:| 物质 | N2 | H2 | NH3 |
| 起始浓度(摩/升) | a | 6 | 0 |
| 转化浓度(摩/升) | b | c | d |
| 平衡浓度(摩/升) | 1 | e | 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
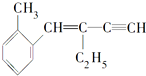
| A、该有机物分子式为C13H16 |
| B、该有机物属于苯的同系物 |
| C、该有机物分子至少有4个碳原子共直线 |
| D、该有机物分子最多有13个碳原子共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、MgO、NO2、NO |
| B、MgO、NO2、O2 |
| C、Mg(NO2)2、O2 |
| D、MgO、N2O3、O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、宁波从2012年3月25日起公布了空气中的PM2.5,PM2.5是指空气中细颗粒物直径≤2.5u m(1um=10-6m)的颗粒物,它在空气中能形成气溶胶 |
| B、“可燃冰”的燃烧、从海水中得到溴单质、石油分馏全都是化学变化的过程 |
| C、氯化钠、干冰、纯碱属于晶体,具有规则的几何外形和固定的熔点,石蜡、玻璃属于非晶态物质,没有固定的熔点,也不具备规则的几何外形 |
D、原子结构模型的演变历史可表示为: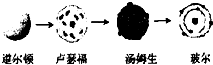 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com