A
分析:A、根据NO
2和N
2O
4的分子组成分析;
B、求出D
2O的物质的量,根据D
2O的原子结构计算;
C、首先判断乙醇在标况下的聚集状态;
D、从酸分为一元酸、二元酸和多元酸的角度分析.
解答:A、NO
2和N
2O
4的分子N和O原子的个数比值相同,都是1:2,含原子的数目相同,为
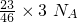
=1.5N
A,故A正确;
B、1个分子中含有电子数目为:2×1+8=10,8g D
2O的物质的量为:
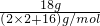
=
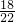
mol,则18gD
2O所含电子数目小于10N
A,故B错误;
C、标准状况下,乙醇为液态,无法计算物质的量,故C错误;
D、酸分为一元酸、二元酸和多元酸等,1Lmol?L
-1的两种强酸溶液中,所含氢离子数目均≥N
A,故D错误.
故选A.
点评:本题考查阿伏加德罗常数知识,题目难度不大,注意物质的组成、结构、状态、性质及存在条件等.

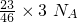 =1.5NA,故A正确;
=1.5NA,故A正确;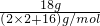 =
=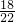 mol,则18gD2O所含电子数目小于10NA,故B错误;
mol,则18gD2O所含电子数目小于10NA,故B错误;
