
����Ŀ��֯��Ư����������(NaClO2)����Һ�п�����ClO2��HClO2��ClO![]() ��Cl���ȣ�����HClO2��ClO2������Ư�����ã���ClO2���ж����塣25 ��ʱ������ֺ�����pH�仯�����ͼ��ʾ(Cl��û�л���)������˵���������
��Cl���ȣ�����HClO2��ClO2������Ư�����ã���ClO2���ж����塣25 ��ʱ������ֺ�����pH�仯�����ͼ��ʾ(Cl��û�л���)������˵���������

A. 25 ��ʱ��HClO2�ĵ���ƽ�ⳣ������ֵKa��10��6
B. ʹ�ø�Ư�������pHΪ3.0
C. 25 ��ʱ����Ũ�ȵ�HClO2��Һ��NaClO2��Һ�������Ϻ����Һ�У�c(HClO2)��2c(H��)��c(ClO![]() )��2c(OH��)
)��2c(OH��)
D. ���¶��µ�NaClO2��Һ��c(Na��)��c(ClO![]() )>c(OH��)>c(H��)
)>c(OH��)>c(H��)
���𰸡�B
��������A. ��ͼ���֪����pH=6ʱ��c(H+)=10-6mol/L��c(HClO2)=c(ClO2-)����ˣ�25 ��ʱ��HClO2�ĵ���ƽ�ⳣ������ֵKa��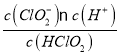 =10��6��A��ȷ��B.������֪HClO2��ClO2������Ư����������ClO2���ж����壬��ͼ���֪����pH=4��4.5ʱ��Ư�������B����ȷ��C. 25 ��ʱ����Ũ�ȵ�HClO2��Һ��NaClO2��Һ�������Ϻ��ɵ���غ��c(Na+)+c(H+)= c(ClO
=10��6��A��ȷ��B.������֪HClO2��ClO2������Ư����������ClO2���ж����壬��ͼ���֪����pH=4��4.5ʱ��Ư�������B����ȷ��C. 25 ��ʱ����Ũ�ȵ�HClO2��Һ��NaClO2��Һ�������Ϻ��ɵ���غ��c(Na+)+c(H+)= c(ClO![]() )��c(OH��)���������غ��2c(Na+)= c(HClO2)��c(ClO
)��c(OH��)���������غ��2c(Na+)= c(HClO2)��c(ClO![]() )�����Ի����Һ��c(HClO2)��2c(H��)��c(ClO
)�����Ի����Һ��c(HClO2)��2c(H��)��c(ClO![]() )��2c(OH��)��C��ȷ��D. NaClO2��Һ�У�����ClO
)��2c(OH��)��C��ȷ��D. NaClO2��Һ�У�����ClO![]() ����ˮ��ʹ��Һ�ʼ��ԣ����Ը��¶��µ�NaClO2��Һ��c(Na��)��c(ClO
����ˮ��ʹ��Һ�ʼ��ԣ����Ը��¶��µ�NaClO2��Һ��c(Na��)��c(ClO![]() )>c(OH��)>c(H��)��D��ȷ������ѡB��
)>c(OH��)>c(H��)��D��ȷ������ѡB��


 ��Ǭ����������ҵ���ּ����ӱ����������ϵ�д�
��Ǭ����������ҵ���ּ����ӱ����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2015��8��12�գ�������������ը�¹�ȷ�����軯����NaCN�����������Ƶȣ��軯�ƶ��Ժ�ǿ����ˮ���������ж���ȼ�軯����HCN�����塣�軯��ķе�ֻ��26 ��������൱���ӷ������������ʹ���������ж��ķ��ա�ͬʱ�軯�������������ƻᷢ����ը���ش���������:
��1��д���軯����ˮ�����軯����������ӷ���ʽ_________________________
��2����ը�ֳ�Լ700�ֵ��軯�ƴ�Լ��Ҫ900�ֵ�˫��ˮ���������軯����˫��ˮ�������ͷų�����ͬʱ������ɫ���壬ʹ���軯�ƵĶ��Դ�ͣ�д���軯����˫��ˮ��Ӧ�Ļ�ѧ����ʽ________________________________��
��3����ը�����ڷ�ˮ�е�CN��������Cr2O![]() �������ⶨ�������̽��з�ˮ������
�������ⶨ�������̽��з�ˮ������
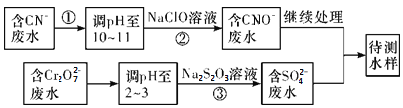
������������ˮ��������Ҫʹ�õķ�����____________
a����������������b���кͷ���������c����������������d��������ԭ��
�ڢ��з�Ӧ��������ų����÷�Ӧ�����ӷ���ʽΪ_________________��
�۲�����У�ÿ����0.4 mol Cr2O![]() ʱת�Ƶ���2.4 mol���÷�Ӧ�����ӷ���ʽ_________��
ʱת�Ƶ���2.4 mol���÷�Ӧ�����ӷ���ʽ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ۺϴ�������ҵ���ϡ��������ڱ�����������Լ��Դ�� 
��1��Ϊ����ij�����Ĺ�ҵ��������Ҫ��N2��SO2��NO��CO�������������ɷ֣����������ͼ1���̣�
��֪��NO+NO2+2NaOH=2NaNO2+H2O��
2NO2+2NaOH=NaNO3+NaNO2+H2O��
�ٷ����ijɷ�Ϊ���ѧʽ����
��ͨ��������ܹ�����ԭ���� ��
�����ռ������յ�������Ҫ��
�ܴ�����NH4+��ˮʱ��������Ӧ�����ӷ���ʽΪ
��2��ij��ɫ��ҵ��ˮ�п��ܺ���NH4+��Na+��Al3+��Cu2+��Cl����SO42����CO32���������еļ������ӣ�Ϊȷ����ɷ֣��������ʵ�飺
a��ȡ10mL�÷�ˮ���Թ��У�����������Ba��NO3��2��Һ��ϡ���ᣬ��ַ�Ӧ����˵õ�0.04mol��ɫ����������Һ�м���AgNO3��Һ����������
b����ȡ10mL�÷�ˮ���Թ��У��μ�NaOH��Һ������ɫ���������������ӵ�һ������ʼ�������壬��������ȫ�ܽ⣮��������������ʵ��������NaOH��Һ����ı仯��ϵ��ͼ2��ʾ���������dz�����������ܽ����ʧ��
��������ʵ���ͼ�����ݣ�
�ٸ÷�ˮ��һ�����е��������������ӷ��ţ���
��ʵ��������100mL����Ũ�ȵ�NaOH��Һʱ���õ��IJ����������ձ�������������Ͳ�⣬����Ҫ�����������ƣ���
��ͼ��a= ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У���ʹ���Ը��������Һ��ɫ�������ܷ�����ѧ��Ӧʹ��ˮ��ɫ���ǣ� ��
A.��ϩ
B.��
C.�ױ�
D.����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧ��Ϊ�ⶨδ֪Ũ�ȵ�������Һ����������ʵ�飺��1.00mL����������Һ����100mLϡH2SO4��Һ����0.14molL-1��NaOH��Һ�ζ�����ϡH2SO4 25.00mL���ζ���ֹʱ����NaOH��Һ15.00mL��
��1����ѧ����0.14molL-1NaOH����Һ�ζ������ʵ��������£�
A.����ʽ�ζ���ȡϡH2SO4 25.00mL��ע����ƿ�У�����ָʾ����
B.�ô��ⶨ����Һ��ϴ��ʽ�ζ���
C.������ˮϴ�ɾ��ζ���
D.ȡ�¼�ʽ�ζ����ñ���NaOH��Һ��ϴ����Һע���ʽ�ζ��̶ܿ���0������2-3cm�����ٰѼ�ʽ�ζ��̶ܹ��ã�����Һ�����̶���0������0���̶�����
E.���ζ����Ƿ�©ˮ
F.��ȡ��ƿ�����ظ�����һ��
G.����ƿ���ڵζ������棬ƿ�µ�һ�Ű�ֽ���ߵα�ҡ����ƿֱ���ζ��յ㣬����
�ζ���Һ�����ڿ̶�
�ٵζ���������ȷ˳���ǣ��������д�� ( )��( )��D��( ) ��A��( ) ��( ) __________
������ȷŨ�ȵ�ϡH2SO4��Һ������ʹ�õ���Ҫ������ ______
�۹۲��ʽ�ζ��ܶ���ʱ�����ζ�ǰ���ӣ��ζ����ӣ������ᵼ�²�õ�ϡH2SO4��ҺŨ�Ȳⶨֵ ______ ��ѡ����ƫ������ƫ����������Ӱ������
�ܼ���������ᣨϡ��ǰ�����ᣩ��Һ�����ʵ���Ũ�ȣ���������С������λ��_____
����֪����CH3COOH 1mol�Ĵ�����Һ��NaOH(aq)��Ӧ����H=-12.1 kJ��mol-1����HCl1mol ��������NaOH(aq)��Ӧ����H=-55.6 kJ��mol-1����CH3COOH��ˮ��Һ�е������H����______
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݻ�һ�����ܱ������У�����һ������һ������������̼������ѧ��Ӧ��
C(s��+2NO(g��![]() CO2(g��+N2(g����ƽ��ʱc (NO�����¶�T�Ĺ�ϵ����ͼ��ʾ��������˵����ȷ����
CO2(g��+N2(g����ƽ��ʱc (NO�����¶�T�Ĺ�ϵ����ͼ��ʾ��������˵����ȷ����
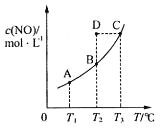
A. �÷�Ӧ����H>0
B. ���÷�Ӧ��T1��T2ʱ��ƽ�ⳣ���ֱ�ΪK1��K2����K1<K2
C����T2ʱ������Ӧ��ϵ����״̬D�����ʱ![]()
D����״̬B��C��D��ѹǿ�ֱ�ΪPB��PC ��PD ���� PC=PD>PB
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڹ�����ռ����Ҫ��λ��
I.�ϳɰ���ҵ�У���ʼʱ���������������ױ�Ϊ1��3ʱ��ÿ��Ӧ1mol N2���ų�92.2kJ��������ͼΪ�ϳɰ���Ӧ�ڲ�ͬ�¶Ⱥ�ѹǿ��ʹ����ͬ���������£�ƽ�������а������������
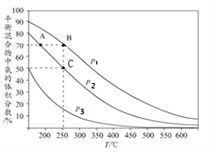
����ͼ��֪��p1��p2��p3�Ĵ�С��ϵΪ________,������_____________________________
��A��B�����ɰ��������ʴ�С��ϵΪ_____________��C�㣬N2��ת����Ϊ_____��
�����й��ںϳɰ���˵����ȷ��_________ (�����)��
A.�Ͽ�1��N��N����ͬʱ��6��N��H���γɣ���Ӧһ���ﵽƽ��״̬
B.��������ƽ����Է����������ٸı�״̬����Ӧһ���ﵽƽ��״̬
C.���ڡ�H<0����S>0���ʺϳɰ���Ӧһ�����Է�����
D.����n(N2):n(H2)�ı�ֵ������������H2��ת����
II.�������Simons�ȿ�ѧ�ҷ����˲���ʹ�����ѻ�Ϊ��Ϳ�ֱ������ȼ�ϵ�صķ��������ط�ӦΪ4NH3+3O2==2N2+6H2O��д�������ĵ缫��Ӧʽ��__________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͨ�����з�ɢϵʱ���ܲ��������������ǣ� ��
A.Fe��OH��3����
B.�Ȼ�����Һ
C.����
D.����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com