
根据Fe3++ Ag  Fe2+
+ Ag+ ,可用Fe3+的盐溶液做刻蚀液将试管中的银镜洗去。
Fe2+
+ Ag+ ,可用Fe3+的盐溶液做刻蚀液将试管中的银镜洗去。
(1)FeCl3溶液显酸性,原因是 (用离子方程式表示)。
(2)关于FeCl3溶液洗银后的相关叙述正确的是 (填序号)。
a.c(Fe3+)减小 b.c(Cl-)不变 c.铁元素质量减小
(3)Fe(NO3)3溶液洗银时,甲同学认为NO3-也能将银氧化。他认为可以通过检验Fe(NO3)3溶液洗银后NO3-的还原产物来判断NO3-是否能将银氧化,而乙同学认为此方法不 可行,乙同学的理由是 。
(4)乙同学欲从洗银废液(Fe3+、 Fe2+、 Ag+、 NO3-)中回收银和刻蚀液,设计了如下路线:
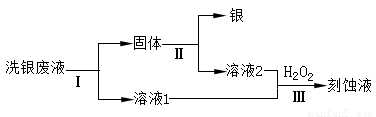
①过程Ⅰ中反应的离子方程式是 。
②过程Ⅱ中加入的试剂可以是 。
(5)镀银后的银氨溶液放置时会析出有强爆炸性的物质,所以不能贮存。从银氨溶液中回收银的方法是:向银氨溶液中加入过量盐酸,过滤,向沉淀AgCl中加入羟氨(NH2OH),充分反应后可得银,羟氨被氧化为N2。
①生成AgCl沉淀的化学方程式是 。
②若该反应中消耗3.3 g羟氨,理论上可得银的质量为 g。
(1)Fe3++3H2O  Fe(OH)3 +3H+ (2)a
Fe(OH)3 +3H+ (2)a
(3)酸性条件下NO3-也可能与Fe2+发生氧化还原反应 (4)①2Fe3++Fe=3Fe2+ Fe+2Ag+=Fe2++2Ag
②稀盐酸或稀硫酸 (5)①Ag(NH3)2OH+3HCl=AgCl↓+2NH4Cl+H2O ②10.8
【解析】
试题分析:(1)FeCl3溶液显酸性是因为铁离子水解生成氢氧化铁和氢离子;反应的离子方程式为:Fe3++3H2O⇌Fe(OH)3+3H+;(2)FeCl3溶液洗银,发生反应为:Fe3++Ag⇌Fe2++Ag+;a.c(Fe3+)减小 故a符合;b. c(Cl-)不变,故b不符合;c.铁元素存在形式不同但质量不会减小,故c不符合;(3)可以通过检验Fe(NO3)3溶液洗银后NO3-的还原产物来判断NO3-是否能将银氧化;同时注意在酸溶液中,亚铁离子也会反应;(4)①洗银废液(Fe3+、Fe2+、Ag+、NO3-)中回收银和刻蚀液需要先加入过量铁,还原Fe3+、Ag+;反应的离子方程式为:2Fe3++Fe=3Fe2+Fe+2Ag+=Fe2++2Ag;②过程Ⅱ中加入的试剂是溶解过量的铁,可以用稀盐酸或稀硫酸;(5)①银氨溶液中加入过量盐酸生成氯化银,同时生成氯化铵和水,反应的化学方程式为:Ag(NH3)2OH+3HCl=AgCl↓+2NH4Cl+H2O;②向沉淀AgCl中加入羟氨(NH2OH),充分反应后可得银,羟氨被氧化为N2.反应为:2AgCl+2NH2OH=N2↑+2Ag+2H2O+2HCl,反应中消耗3.3g羟氨物质的量= =0.1mol,生成银的物质的量0.1mol,质量10.8g。
=0.1mol,生成银的物质的量0.1mol,质量10.8g。
考点:本题考查了盐类水解的应用,回收利用的提取过程盐类分析判断,试剂选择的目的,离子方程式化学方程式书写的方法,掌握物质性质是关键,题目难度中等。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | E |
查看答案和解析>>
科目:高中化学 来源: 题型:
| H | + 4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com