
【题目】FeSO47H2O广泛用于医药和工业领域.以下是FeSO47H2O的实验室制备流程图. 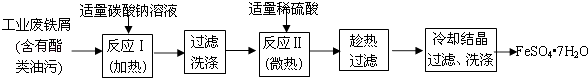
根据题意完成下列填空:
(1)碳酸钠溶液能除去酯类油污,是因为(用离子方程式表示),
(2)废铁屑中含氧化铁,无需在制备前除去,理由是(用离子方程式回答) , . 以下是测定某补血剂(FeSO47H2O)中铁元素含量的流程图.根据题意完成下列填空: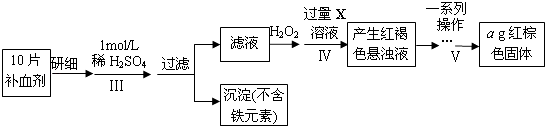
(3)步骤Ⅲ需要100mL1mol/L的稀硫酸,用98.3%,ρ=1.84g/cm3的浓硫酸配制,所用的仪器有量筒、烧杯、玻璃棒、胶头滴管及 .
(4)步骤Ⅴ一系列操作依次是:①过滤②洗涤③④冷却⑤称量⑥恒重操作.操作⑥的目的是 .
(5)假设实验无损耗,则每片补血剂含铁元素的质量g(用含a的代数式表示).
【答案】
(1)CO32﹣+H2O?HCO3﹣+OH﹣
(2)Fe2O3+6H+═2Fe3++3H2O;2Fe3++Fe═3Fe2+
(3)100mL容量瓶
(4)灼烧;确保氢氧化铁完全分解成了氧化铁
(5)0.07a
【解析】解:废铁屑中含有酯类油污,Na2CO3为强碱弱酸盐,CO32﹣水解生成HCO3﹣和OH﹣ , 升高促进CO32﹣水解,碱促进油脂水解,然后过滤洗涤,加入稀硫酸,发生反应II为Fe+H2SO4=FeSO4+H2↑,趁热过滤、冷却结晶,过滤洗涤得到FeSO47H2O;(1)Na2CO3为强碱弱酸盐,CO32﹣水解生成HCO3﹣和OH﹣ , 水解方程式为CO32﹣+H2OHCO3﹣+OH﹣ , 所以答案是:CO32﹣+H2OHCO3﹣和OH﹣;(2)废铁屑中含氧化铁,无需在制备前除去,因为氧化铁和酸反应生成铁盐,铁盐能被Fe还原生成亚铁盐,涉及的离子方程式为Fe2O3+6H+═2Fe3++3H2O、2Fe3++Fe═3Fe2+ , 所以答案是:Fe2O3+6H+═2Fe3++3H2O;2Fe3++Fe═3Fe2+;
将补血剂研细,向药片中加入稀硫酸,然后过滤得到沉淀,向滤液中加入双氧水,发生反应2Fe2++H2O2+2H+=2Fe3++2H2O,向溶液中加入过量X溶液生成红褐色沉淀,则X为碱,将红褐色沉淀灼烧得到红棕色固体Fe2O3 , (3)配制一定物质的量浓度的溶液时还需要100mL容量瓶,所以答案是:100mL容量瓶;(4)步骤Ⅴ一系列操作依次是:①过滤②洗涤③灼烧④冷却⑤称量⑥恒重操作,操作⑥的目的是确保氢氧化铁完全分解成了氧化铁,
所以答案是:灼烧(加热);确保氢氧化铁完全分解成了氧化铁;(5)ag中m(Fe)= ![]() ×ag=0.7ag,则每片药品中Fe的质量为0.07ag,
×ag=0.7ag,则每片药品中Fe的质量为0.07ag,
所以答案是:0.07a.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】以包列科学家Danici Shcchtman因发现准晶体获得2011年诺贝尔化学奖.人们在自然界中也找到了组成为Al63Cu24Fe13的天然准晶体.将相同质量的此准晶体分别与足量的盐酸、烧碱和稀硝酸反应,产生气体的物质的量关系为( )
A.n(烧碱)<n(稀硝酸)<n(盐酸)
B.n(烧碱)<n(盐酸)<n(稀硝酸)
C.n(稀硝酸)<n(烧碱)<n(盐酸)
D.n(盐酸)<n(稀硝酸)<n(烧碱)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CaCO3的摩尔质量为100g/mol,将5.0g CaCO3固体完全溶于稀盐酸后,再用蒸馏水稀释成100mL溶液.该溶液中Ca2+ 的物质的量浓度为( )
A.5.0 mol/L
B.0.50 mol/L
C.1.0 mol/L
D.0.10 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质的量浓度表述正确的是( )
A.0.2mol·L-1Na2SO4溶液中含有Na+和SO42-总物质的量为0.6mol
B.50mL 2mol·L-1的NaCl溶液和100 mL L 0.5mol·L-1MgCl2溶液中,Cl-的物质的量浓度相等
C.用1L水吸收22.4L氯化氢(标况下)所得盐酸的浓度是1mol·L-1
D.10g 98%的硫酸(密度为1.84g·cm-3)与10mL 18.4mol·L-1的硫酸的浓度是相同的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知HClO的酸性比H2CO3弱,下列反应Cl2+H2OHCl+HClO达到平衡后,要使平衡体系中HClO的浓度增大,应采取的方法是( )
A.加入石灰石
B.光照
C.加入固体NaOH
D.加水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,在pH=11的某溶液中,由水电离的c(OH﹣)为( )
①1.0×10﹣7 molL﹣1 ②1.0×10﹣6 molL﹣1
③1.0×10﹣3 molL﹣1 ④1.0×10﹣11 molL﹣1 .
A.③
B.④
C.①或③
D.③或④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列划横线的物质在化学反应中能被完全消耗的是( )
A.标准状况下,将1g铝片投入20mL 18.4molL﹣1的硫酸中
B.向100mL3moIL﹣1的硝酸中加入5.6g铁
C.用50mL18molL﹣1浓硫酸与足量Cu共热(指其中的硫酸被完全消耗)
D.在5×107 Pa、500℃和铁触媒催化的条件下,用3mol氢气和2mol氮气合成氨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.放热的反应发生时不必加热
B.反应是放热还是吸热必须看反应物和生成物所具有的总能量的相对大小
C.需要加热才能发生的反应一定是吸热反应
D.放热反应在常温下一定很容易发生
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com