
科目:高中化学 来源: 题型:阅读理解
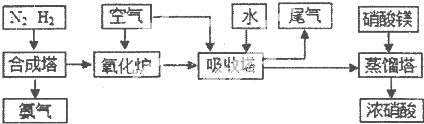
| A | B | C | D | E | |
| n(CO2) | 3 | l | 0 | 1 | l |
| n(H2) | 2 | l | 0 | 1 | 2 |
| n(CO) | 1 | 2 | 3 | 0.5 | 3 |
| n(H2O) | 5 | 2 | 3 | 2 | l |
| T/°C | T1 | 300 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
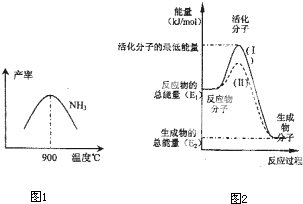
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(2010?厦门二模)为探究NaHCO3、Na2CO3和盐酸(以下盐酸浓度均为1mol?L-1)反应过程中的热效应,进行实验并测得如下数据
|
查看答案和解析>>
科目:高中化学 来源: 题型:
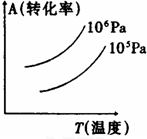 有一化学平衡mA(g)+nB(g)?PC(g)+qD(g),右图表示A的转化率与压强、温度的关系.由此得出的正确结论是( )
有一化学平衡mA(g)+nB(g)?PC(g)+qD(g),右图表示A的转化率与压强、温度的关系.由此得出的正确结论是( )| A、正反应是吸热反应 | B、(m+n)<(p+q) | C、压强增大,A的转化率减小 | D、温度升高,A的转化率减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com