
【题目】化学反应原理在生产和生活中有广泛的应用。
Ⅰ.NO2与SO2都是形成酸雨的主要物质。在一定条件下,两者能发生反应:
NO2(g)+SO2(g)![]() SO3(g)+NO(g)
SO3(g)+NO(g)
(1)在一定条件下,将等物质的量的NO2、SO2气体置于体积固定的密闭容器中发生反应,下列能说明反应已经达到平衡状态的是
a.v(NO2)生成=v(SO2)消耗
b.混合气体的总压强不再改变
c.容器内气体颜色不再改变
d.容器内气体平均相对分子质量不再改变
(2)科学家正在研究利用催化技术将NO2和CO转变成无害的CO2和N2,反应的化学方程式:
2NO2(g)+4CO(g)![]() 4CO2(g)+N2(g)+Q(Q>0)
4CO2(g)+N2(g)+Q(Q>0)
若在密闭容器中充入NO2和CO,下列措施能提高NO2转化率的是 。
A.选用高效催化剂 B.充入NO2 C.降低温度 D.加压
Ⅱ.(1)17℃、1.01×105Pa,在2L密闭容器NO2和N2O4的混合气体达到平衡时,NO2的物质的量为0.2mol,N2O4的体积分数为6/11。计算该条件下反应2NO2(g)![]() N2O4(g)的平衡常数K= 。若此时向容器中再充入0.1mol NO2和0.12mol N2O4,原化学平衡 移动(填“正向”、“逆向”或“不”)。
N2O4(g)的平衡常数K= 。若此时向容器中再充入0.1mol NO2和0.12mol N2O4,原化学平衡 移动(填“正向”、“逆向”或“不”)。
(2)现用一定量的Cu与足量的浓HNO3反应,制得2.20L(已折算到标准状况)已达到平衡的NO2 和N2O4的混合气体,理论上至少需消耗Cu g(保留两位小数)。
【答案】Ⅰ.(1)a、c(2分)(2)C、D(2分)
Ⅱ.(1)12(2分)正向(2分)(2)4.86g(2分)
【解析】
试题分析:Ⅰ、(1)a.v(NO2)生成=v(SO2)消耗表示正逆反应速率相等,反应达到平衡状态,a正确;b.反应前后体积不变,因此压强始终不变,则混合气体的总压强不再改变不能说明反应达到平衡状态,b错误;c.容器内气体颜色不再改变说明NO2浓度不再发生变化,反应达到平衡状态,c正确;d.混合气的平均相对分子质量是混合气的质量和混合气的总的物质的量的比值,质量和物质的量均不变,因此容器内气体平均相对分子质量始终不变,不能说明反应达到平衡状态,d错误,答案选ac;
(2)A.选用高效催化剂不能改变平衡状态,A错误;B.充入NO2平衡向正反应方向进行,但NO2转化率降低,B错误;C.正反应放热,降低温度平衡向正反应方向进行,NO2转化率升高,C正确;D正反应体积减小,增大压强平衡向正反应方向进行,NO2转化率增大,D正确,答案选CD;
Ⅱ.(1)平衡时N2O4是xmol,则![]() ,解得x=0.24,因此平衡时NO2和N2O4的浓度分别是0.1mol/L、0.12mol/L,则该温度下反应2NO2(g)
,解得x=0.24,因此平衡时NO2和N2O4的浓度分别是0.1mol/L、0.12mol/L,则该温度下反应2NO2(g)![]() N2O4(g)的平衡常数K=
N2O4(g)的平衡常数K=![]() ;若此时向容器中再充入0.1mol NO2和0.12mol N2O4,则此时NO2和N2O4的浓度分别是0.15mol/L、0.18mol/L,浓度熵=
;若此时向容器中再充入0.1mol NO2和0.12mol N2O4,则此时NO2和N2O4的浓度分别是0.15mol/L、0.18mol/L,浓度熵=![]() <12,因此原化学平衡正向移动。
<12,因此原化学平衡正向移动。
(2)由(1)可知,达到平衡时,2.20L混合气体中:V(N2O4)=2.2L×6/11=1.2L,所以NO2体积是1L,则 相当于NO2的体积是1.2L×2+1L=3.4L,NO2的物质的量是0.152mol,转移电子的物质的量是0.152mol,根据电子转移守恒可知消耗铜的物质的量是0.152mol÷2=0.076mol,质量是4.86g。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g) ΔH=Q kJ/mol(Q>0),某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是
Si(s)+4HCl(g) ΔH=Q kJ/mol(Q>0),某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1 mol, 则达平衡时,吸收热量为Q kJ
C.反应至4 min时,若HCl浓度为0. 12 mol/L,则H2的反应速率为0.03 mol/(L·min)
D.当反应吸收热量0.025Q kJ时,生成的HCl通入含0. 1 mol NaOH的溶液恰好反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含 SO32-、Fe2+、Br-、I-各 0.1 mol 的溶液中通入标准状况下的 Cl2,通入 Cl2的体积和溶液中相关离子的物质的量的关系图正确的是
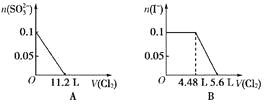
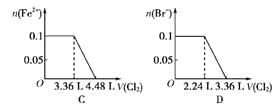
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于元素周期表的叙述,错误的是( )
A.第IA族元素全部是金属元素
B.过渡元素全是金属元素
C.第ⅦA族元素是同周期中非金属性最强的元素
D.在元素周期表中金属与非金属的分界线附近可以寻找制造半导体的材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,氧化剂与还原剂物质的量之比为1∶2的是
A.3S+6NaOH=2Na2S+Na2SO3+3H2O
B.2CH3COOH+Ca(ClO)2=2HClO+Ca(CH3COO)2
C.l2+2NaC1O3=2NaIO3+Cl2
D.4HCl(浓)+MnO2![]() MnCl2十Cl2↑+2H2O
MnCl2十Cl2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是 ( )
A. 物质燃烧不一定是放热反应
B. 放热反应不需要从外界吸收任何能量就能发生
C. 在一个确定的化学反应中,反应物总能量总是高于生成物总能量
D. 化学反应除了生成新的物质外,还伴随着能量的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】

(1)写出仪器D、E的名称 、 .
(2)分离以下混合物应该主要选用使用什么仪器?(填字母符号)粗盐和泥沙 ;菜籽油和水 。
(3)计算标签上硫酸的物质的量浓度为 。
(4)用18 mol·L-l 浓硫酸配制100 ml 3.0 mol·L-l 稀硫酸的实验步骤如下:① 计算所用浓硫酸的体积;②量取一定体积的浓硫酸;③ 溶解;④ 转移、洗涤;⑤ 定容、摇匀。回答下列问题:

Ⅰ.所需浓硫酸的体积是 ,量取浓硫酸所用的量筒的规格是
(从下列量筒的规格中选用 A 10mL B 20mL C 50mL D 100mL)
Ⅱ.第③步实验的操作是 。
Ⅲ.下列情况对所配制的稀硫酸浓度有何影响?(用偏大、偏小、无影响填写)
A.所用的浓硫酸长时间放置在密封不好的容器中
B.量取浓硫酸时仰视
C.容量瓶用蒸馏洗涤后残留有少量的水
D.所用过的烧杯、玻璃棒未洗涤
(5)浓度不等的两种硫酸溶液等质量混合后,溶液的质量分数为a%,而等体积混合后,溶液的质量分数为b%;浓度不等的两种氨水等质量混合后,其质量分数为a%,而等体积混合后,溶液的质量分数为c%,那么a、b、c数值的关系是( )
A.a>b>c B.b>a>c C.c>b>a D.c>a>b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨的化合物合成、应用及氨的固定一直是科学研究的热点。
(1)以CO2与NH3为原料合成化肥尿素的主要反应如下:
①2NH3(g)+CO2(g)=NH2CO2NH4(s);ΔH=-159.47kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g);ΔH=akJ·mol-1
③2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g);ΔH=-86.98kJ·mol-1
则a为______________。
(2)反应2NH3(g)+CO2(g)![]() CO(NH2)2(l)+H2O(g)在合成塔中进行。下图中Ⅰ、Ⅱ、Ⅲ三条曲线为合成塔中按不同氨碳比 [n(NH3)/n(CO2)]和水碳比[n(H2O)/n(CO2)]投料时二氧化碳转化率的情况。
CO(NH2)2(l)+H2O(g)在合成塔中进行。下图中Ⅰ、Ⅱ、Ⅲ三条曲线为合成塔中按不同氨碳比 [n(NH3)/n(CO2)]和水碳比[n(H2O)/n(CO2)]投料时二氧化碳转化率的情况。

①曲线Ⅰ、Ⅱ、Ⅲ水碳比的数值分别为:
A.0.6~0.7 B.1~1.1 C.1.5~1.61
生产中应选用水碳比的数值为 ___________(选填序号)。
②生产中氨碳比宜控制在4.0左右,而不是4.5的原因可能是 。
(3)尿素可用于湿法烟气脱氮工艺,其反应原理为:
NO+NO2+H2O=2HNO2;2HNO2+CO(NH2)2=2N2↑+CO2↑+3H2O。
①当烟气中NO、NO2按上述反应中系数比时脱氮效果最佳。若烟气中V(NO)∶V(NO2)=5∶1时,可通入一定量的空气,同温同压下,V(空气)∶V(NO)= (空气中氧气的体积含量大约为20%)。
②下图是尿素含量对脱氮效率的影响,从经济因素上考虑,一般选择尿素浓度约为_________%。

(4)下图表示使用新型电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制造出既能提供能量,同时又能实现氮固定的新型燃料电池。请写出该电池的正极反应式___________________。生产中可分离出的物质A的化学式为 。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com