
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
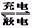 Ag2O+Zn+2H2O,此电池放电时,负极上发生反应的物质是( )
Ag2O+Zn+2H2O,此电池放电时,负极上发生反应的物质是( )| A.Ag | B.Zn(OH)2 | C.Ag2O | D.Zn |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.正极电极反应:O2+2H2O+4e-====4OH- |
B.负极电极反应:CH3OH+8OH--6e-====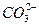 +6H2O +6H2O |
| C.电池在使用过程中电解质溶液的pH升高 |
| D.当外电路通过0.6 mol电子时,理论上消耗甲醇3.2 g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Zn为正极,Ag2O为负极 | B.Zn为负极,Ag2O为正极 |
| C.原电池工作时,正极区溶液PH值减小 | D.原电池工作时,负极区溶液PH值增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CH4在负极发生氧化反应 |
| B.O2作为氧化剂发生还原反应 |
| C.甲烷燃料电池实现了化学能转变为电能 |
| D.分别将1molH2和CH4做燃料电池的原料,产生电量一样多 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.负极反应式为CH4+10OH--8e=CO32-+7H2O |
| B.正极反应式为O2+2H2O+4e=4OH- |
| C.随着不断放电,电解质溶液碱性不变 |
| D.甲烷燃料电池的能量利用率比甲烷燃烧的能量利用率大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 K2S4+3KI。装置(Ⅱ)为电解池的示意图。当闭合开关K时,X附近溶液先变红。则下列说法正确的是
K2S4+3KI。装置(Ⅱ)为电解池的示意图。当闭合开关K时,X附近溶液先变红。则下列说法正确的是
| A.闭合K时,K+从右到左通过离子交换膜 |
| B.闭合K时,A的电极反应式为:3I--2e-=I |
| C.闭合K时,X的电极反应式为:2Cl--2e-=Cl2↑(Ⅱ) |
| D.闭合K时,当有0.1 mol K+通过离子交换膜,X电极上产生标准状况下气体1.12 L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
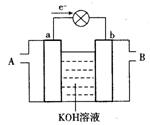
| A.A处通人的是空气,B处通人的是水煤气 |
| B.a电极发生还原反应,b电极发生氧化反应 |
C.a电极的反应式包括:CO+4OH-+2e-=CO +2H2O +2H2O |
| D.如用这种电池电镀铜,待镀金属增重6.4 g,则至少消耗标准状况下的水煤气2.24 L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com