
(16分)按要求回答问题:
(1)写出对应的化学方程式:
Cu2++Fe=Cu+Fe2+_________________________
CO32-+2H+ =CO2↑+H2O__________________________
(2)写出对应的离子方程式:
碳酸氢钙溶液与氢氧化钠溶液反应_________________
铁与氯化铁溶液反应
(3)写出下列物质的电离方程式:
硫酸铝电离的电离方程式:
KHCO3电离的电离方程式:
(4)用双线桥法标出电子转移的方向和数目:
2FeCl3 + 2KI = 2FeCl2 + 2KCl + I2
5NH4NO3 = 4N2↑+ 9H2O + 2HNO3
(1)CuSO4+Fe=Cu+FeSO4 Na2CO3+2HCl=2NaCl+CO2↑+H2O
(2)Ca2++2HCO3-+2OH-=CaCO3 ↓+2H2O + CO32- Fe+2Fe3+=3Fe2+
(3)Al2(SO4)3=2Al3++3SO42- KHCO3 = K+ + HCO3-

【解析】
试题分析:(1)Cu2++Fe=Cu+Fe2+表示可溶性Cu盐与金属铁反应,化学方程式可以为CuSO4+Fe=Cu+FeSO4;CO32-+2H+ =CO2↑+H2O表示可溶性碳酸盐和强酸反应,化学方程式可以为Na2CO3+2HCl=2NaCl+CO2↑+H2O。
(2)碳酸氢钙溶液与氢氧化钠溶液反应的离子方程式为Ca2++2HCO3-+2OH-=CaCO3 ↓+2H2O+CO32-;铁与氯化铁溶液反应的离子方程式为Fe+2Fe3+=3Fe2+。
(3)硫酸铝电离的电离方程式为:Al2(SO4)3=2Al3+=3SO42-;KHCO3电离的电离方程式为KHCO3=K++HCO3-。
(4)双线桥

考点:离子方程式的书写
点评:本题考查化学方程式、离子方程式、电离方程式和双线桥的书写,非常基础简单。


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| T/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
| n(NH3) |
| n(CO2) |

| OH- |
| H+ |
| c(HCO3-):c(H2CO3) | 1.0 | 17.8 | 20.0 | 22.4 |
| pH | 6.10 | 7.35 | 7.40 | 7.45 |
查看答案和解析>>
科目:高中化学 来源: 题型:
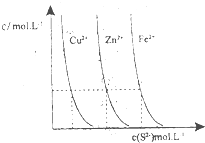 以下是对化学反应变化过程及结果的研究.按要求回答问题:
以下是对化学反应变化过程及结果的研究.按要求回答问题:| 弱酸化学式 | CH3COOH | HCN | H2CO |
| 电离平衡常数(25℃) | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K1=5.6×10-11 |
| 放电 |
| 通电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
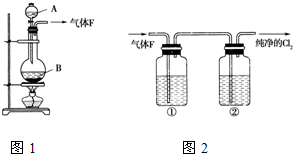
查看答案和解析>>
科目:高中化学 来源: 题型:
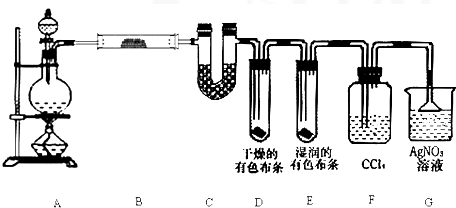
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com