
����Ŀ��ij�о�С��Ϊ̽���������绯ѧ��ʴ��Ӱ�����أ�����Ͼ��ȵ��������ۺ�̼��������ƿ�ײ�������ƿ��(��ͼ1)���ӽ�ͷ�ι��е��뼸�δ�����Һ��ͬʱ���������е�ѹǿ�仯(�����ͼ2)������������������

A��ͼ2�У�t2ʱ������ѹǿ����С����ʼѹǿ����Ϊ���۷�����������ʴ
B��̼�۱���ĵ缫��Ӧʽֻ�У�2H2O + O2 + 4e-== 4OH-
C��̼�۱���һ�������˻�ԭ��Ӧ
D��ͼ3�У�������ʴʱ����ת�Ʒ������ͷ��ʾ

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������(Na2S2O5)�dz��õ�ʳƷ��������֮һ��ij�о�С���������ʵ�飺
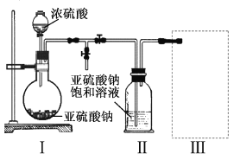
ʵ��һ���������Ƶ���ȡ
������ͼװ��(ʵ��ǰ�ѳ���װ���ڵĿ���)��ȡNa2S2O5��װ��II����Na2S2O5���������������ķ�ӦΪ��
Na2SO3��SO2��Na2S2O5
��1��װ��I�в�������Ļ�ѧ����ʽΪ ��
��2��Ҫ��װ��II�л���������ľ��壬�ɲ�ȡ�ķ��뷽���� ��
��3��װ��III���ڴ���β������ѡ�õ������װ��(�г���������ȥ)Ϊ ��(�����)��
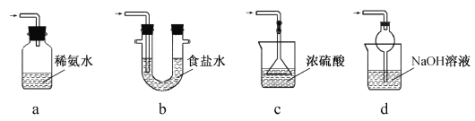
ʵ������������Ƶ�����
Na2S2O5����ˮ������NaHSO3��
��4������Na2S2O5�����ڿ������ѱ�������ʵ�鷽���� ��
ʵ�������Ѿ��п��������������IJⶨ
��5�����ѾƳ���Na2S2O5�������������ⶨij���Ѿ��п��������IJ�����(������SO2����)�ķ������£�

(��֪������еĶ��������ڵ����ˮʱ�����ķ�ӦΪ
SO2��I2��2H2O��H2SO4��2HI)�ڲⶨʱ������0.01mol��L��1��I2��Һ25.00 mL���ô�ʵ������Ʒ�п��������IJ�����(������SO2����)Ϊ g��L��1��������ʵ������У����в���HI���������������ý�� (�ƫ�ߡ���ƫ�͡����䡱)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��G�Ǽ������ķ������ģ��(��ͼ)���ݴ˻ش��������⣺


��1�������º�̼����ߵ���̬����________(����ĸ)��
��2���ܹ������ӳɷ�Ӧ������________�֡�
��3��һ±��������������________(��д��ĸ)��
��4��д��ʵ������D�Ļ�ѧ����ʽ��
_____________________________________________________________
��5��д��F����������Ӧ�Ļ�ѧ����ʽ��
_____________________________________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ����ۼӵ�ʳ���к��е���ء���֪�������������������һ�ֽ�ǿ��������������⻯��������εȻ�ԭ�����ʷ�Ӧ����ҵ��������ص��������£�
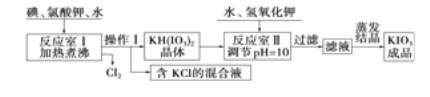
��ش��������⣺
��1����֪��Ӧ���������ķ�Ӧ�У����ֻ�ԭ�������õ�������ͬ����д���÷�Ӧ�Ļ�ѧ����ʽ�� ��
��2����Ӧ�����������У���Ŀ���ǣ����ӿ췴Ӧ���ʣ�ʹ��Ӧ���ַ�Ӧ���� ����ӻ�ѧƽ��ǶȽ�������
��3����֪�������ʵ��ܽ�ȼ��±���
KCl | KH(IO3)2 | KClO3 | |
�ܽ��g/100 gˮ(25 ��) | 20.8 | 0.8 | 7.5 |
�ܽ��g/100 gˮ(80 ��) | 37.1 | 12.4 | 16.2 |
���ϱ����ݷ�����֪��������������Ϊ �� ��
��4���ڷ�Ӧ�����м���KOH������Һ��pH��10����Ŀ���� ��
��5����ͬѧ���ⶨ��Ʒ�е���صĺ��������������ʵ�飺
��ȷ��ȡ1 g��Ʒ������������ˮʹ����ȫ�ܽ⣻
����ϡ�����ữ����������Һ���������KI��Һ����ֽ��裻
���Ե���Ϊָʾ������μ���2.0 mol��L��1��Na2S2O3��Һ������ɫ�պ���ȥʱ������Na2S2O3��Һ12.00 mL�����Ʒ��KIO3����������Ϊ ����ʽ���������������λ��Ч���֣�
(��֪��KIO3��5KI��3H2SO4===3K2SO4��3I2��3H2O��I2��2Na2S2O3===2NaI��Na2S4O6)��
��6����ͬѧ�ֶԴ�����NaCl������KIO3������������ʵ�飺
�������� | ʵ������ |
ȡ1g������NaCl����3mLˮ�����Һ�� | ��Һ�ޱ仯 |
����5�ε�����Һ��1mL 0.1mol/L KI��Һ���� | ��Һ�ޱ仯 |
Ȼ���ٵ���1��1mol/L��H2SO4���� | ��Һ����ɫ |
�����Ʋ�ʵ���в�����ɫ����Ŀ���ԭ�������ӷ���ʽ��ʾ ��
��������ͬѧ��ʵ�����Ʋ⣬��ͬѧ��ʵ������ (����ƫ��������ƫС��������Ӱ����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ס����ȡ������ũҩ�е���Ҫ���Ԫ�ء���ش��������⣺
��1����̬��ļ۵����Ų�ʽ��___________________________��
��2��������PH3�е�ߵ�ԭ����______________________��
��3�������йص����ס����ȵ�˵����ȷ����__________��
a����һ��������С�����˳����S��P��Cl
b��PO43-��SO42-��ClO4-��Ϊ�ȵ����壬���ǵĿռ乹�;�Ϊ������
c���ס����Ȼ�̬ԭ�ӵ�δ�ɶԵ�������������
d��1mol(C2H5O)P=0�����к��е���������ĿΪ24��6.02��1023
��4����������������ܵ��߶ȹ�ע�����¡���ĥͿ�ϣ����߽ṹ���ơ������ṹ��ͼ��ʾ������������ÿ����ԭ����Χ�����������ԭ����ĿΪ__________������ṹ�д��ڵĻ�ѧ����_______(�����)��

a�����Ӽ�b�����ۼ�c�����Ӽ�������d����λ��
����������۵�Ҫ��������ߣ���ԭ��______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�����ڱ��й� �����У� ���壬�� ���У��� �����ڣ����� �������ڣ� �������ڣ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com